实验室可用氯酸钾或过氧化氢制取氧气。
(1)氯酸钾制取氧气的过程看表示如下:氯酸钾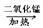 氯化钾+氧气
氯化钾+氧气
①上述反应中氯元素从______价变成-1价。
②上述反应中二氧化锰的作用是__________,如果不加二氧化锰,该反应能进行吗?_____________(填“能”或“不能”)。
(2)用过氧化氢制取氧气的化学方程式可表示为:
2H2O2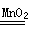 2H2O+ O2↑
2H2O+ O2↑
①H2O2、H2O是不同物质,其原因是________________。
②若实验室要制取16g氧气,至少需要过氧化氢多少克?(写出计算过程)
锌是人体生长发育不可缺少的微量元素。葡萄糖酸锌是一种常用的补锌剂。请回答下列问题:
(1)葡萄糖酸锌由种元素组成。
(2)葡萄糖酸锌中所含锌元素的质量分数为(不要求写出计算过程,结果精确到0.1%)。
取碳酸钠和氯化钠的混合物10g,投入50g溶质质量分数为9.8%的稀硫酸中,恰好完全反应,假设生成的气体全部逸出。计算:
(1)反应中生成二氧化碳气体的质量;
(2)该混合物中碳酸钠的质量分数。
(提示:反应的化学方程式为
)
黄铜是铜、锌合金,它可用来制造机器、电器零件及日用品。为测定某黄铜中铜的质量分数,现取10g该样品粉碎,加入到50g稀硫酸中,恰好完全反应,测得剩余固体质量为3.5g。计算:
(1)黄铜样品中铜的质量分数。
(2)稀硫酸中溶质的质量分数。
向202克硫酸铜溶液中加入一定量铁粉恰好完全反应,经过滤、烘干,得到干燥的固体物质16克。试求:原加入的铁粉质量是多少?最后得到溶液的溶质质量分数是多少?
某学生在课外活动中用铁粉(含杂质且杂质不参加反应)和稀硫酸反应制
取氢气。所做5次实验结果记录如下表(每次实验产生的氢气全部被收集,且体积在相同
条件下测定。该条件下氢气的密度是0.089∥L),
根据上述实验结果进行分析、计算,并回答下列问题:
(1)上述实验中,铁粉一定过量的实验编号是;
(2)铁粉的纯度是;
(3)计算稀硫酸的质量分数(要求写出计算过程,计算结果精确到0.1)。