金属钛(Ti)性能优越,被称为继铁、铝后的“第三金属”。工业上以金红石为原料制取Ti的反应为
aTiO2+bCl2+cC aTiCl4+cCO反应(1)
aTiCl4+cCO反应(1)
TiCl4+2Mg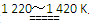 Ti+2MgCl2反应(2)
Ti+2MgCl2反应(2)
关于反应(1)、(2)的分析不正确的是( )
①TiCl4在反应(1)中是还原产物,在反应(2)中是氧化剂;
②C、Mg在反应中均为还原剂,被还原;
③在反应(1)、(2)中的还原性C>TiCl4,Mg>Ti;
④a=1,b=c=2;
⑤每生成19.2 g Ti(Mr=48),反应(1)、(2)中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②⑤
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子可能是()
| A.H+、Mg2+、Al3+ | B.Mg2+、Al3+、Fe3+ |
| C.H+、Ba2+、Al3+ | D.Na+、Mg2+、Al3+ |
设阿伏加德罗常数为NA,下列说法正确的是()
| A.在标准状况下,2.24 L H2O中含有0.1 NA个水分子 |
| B.0.1mol/LNaCl溶液中含有Na+子数为0.1NA |
| C.1molFe与足量盐酸完全反应, Fe失去的电子数为3NA |
| D.在标准状况下,1molH2含有的原子数为2NA |
取四线湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加浓硝酸、浓硫酸、新制氯水、浓氨水,四张试纸最后呈现的颜色是()
| A.白、黑、白、蓝 | B.白、红、白、蓝 | C.白、白、白、蓝 | D.红、黑、红、蓝 |
生产自来水是要用氯气消毒。市场上某些不法商贩为牟取暴利,用自来水冒充纯净水出售。为辨别真假,可用下列试剂来鉴别。该试剂是(C)
| A.酚酞 | B.氯化钠 | C.硝酸银 | D.氢氧化钠 |
实验中在对某种样品进行检验时,加入试剂顺序的不同对最后结果的判断具有很大影响。某样品中可能含有SO42-,实验中加入试剂种类和顺序正确的是( B )
A.BaCl2溶液,稀盐酸B.稀盐酸,BaCl2溶液
C.BaCl2溶液,稀硝酸D.稀硝酸,BaCl2溶液