常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是____________;所含阴离子相同的两种盐的化学式是__________________。
(2)D的化学式为__________________,D溶液显碱性的原因是_________________(用离子方程式表示)。
(3)A和C的溶液反应的离子方程式是______________________________________;
E和氨水反应的离子方程式是____________________________________________。
(4)若要检验B中所含的阳离子,正确的实验方法是______________________________。
(10分)在80℃时,将0.40 mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s n/mol |
0 |
20 |
40 |
60 |
80 |
100 |
| n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
| n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)计算20~40 s内用N2O4表示的平均反应速率为________。
(2)计算在80℃时该反应的平衡常数K=________(请注明单位)。
(3)反应进行至100 s后将反应混合物的温度降低,混合气体的颜色________(填“变浅”、“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有________(填序号)。
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(5)下图是80℃时容器中N2O4物质的量的变化曲线,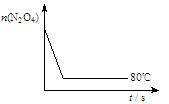
请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。
(12分)通常情况下,微粒A和B为分子,C为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D。假定B的水溶液(B·H2O)和盐酸充分反应后的溶液为E。请用有关的化学式或微粒符号填空:
(1)用化学符号表示下列4种微粒:A:______;B:______;C:______;D:______。
(2)若E溶液中只有一种溶质,则该溶质中包含的化学键类型是:________,_________。电子式为:___________。该溶液中有关离子浓度的大小为:____________________。
(3)若E溶液是由体积相等的稀盐酸和B的水溶液混合而成,且恰好呈中性,则混合前c(HCl)________c(B·H2O)(填“大于”、“小于”或“等于”,下同);混合前盐酸中c(H+)和B·H2O中c(OH-)的关系为c(H+)________c(OH-)。
下图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用下式表示: .
.
(1)上式中X物质的化学式为。
(2)在上述反应中,氧化剂为,氧化产物为,
将两者的氧化性比较,的氧化性更强。
(3)用双线桥法表示该反应的电子转移情况 。
(4)该反应的离子方程式为。
在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有氧化性的是,
只有还原性的是 ,既有氧化性又有还原性的是_。
现有四瓶贴有A、B、C、D标签的溶液,它们可能是K2CO3、Ba(NO3)2、NaHSO4和K2SO4溶液。现进行如下实验,并记录部分现象(如下图)。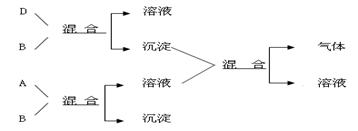
判断A是(写化学式,下同),B是,C是,D是。
B和D反应的离子方程式是
A和B反应的离子方程式。