反应N2O4(g)  2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是( )
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是( )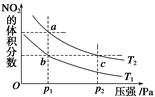
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a深、c浅 |
| C.a、b两点气体的平均相对分子质量:a>b |
| D.b、c两点化学平衡常数:b<c |
为了防止气候变暖的进一步恶化,联合国环境保护组织于1998年通过大会要求各国减少工业排放量的气体是
| A.二氧化硫 | B.二氧化碳 | C.硫化氢 | D.氟里昂 |
下列反应过程需要吸收热量的是
| A.燃烧 | B.浓硫酸溶于水 | C.酸碱中和 | D.水的电离 |
下列反应属于氮的固定的是
①N2和H2在一定条件下反应生成NH3
②雷雨闪电时空气中的N2和O2化合生成NO
③NH3经过催化氧化生成NO
④NH3和HNO3反应生成NH4NO3
| A.①③ | B.②④ | C.③④ | D.①② |
下列变化属于化学变化的是
| A.氨的液化 | B.氯化铵受热“升华” | C.碘的升华 | D.硝酸的挥发 |
2.1g镁铝合金完全溶于足量盐酸,生成氢气2.24L(标准状况下),再向溶液中加入氢氧化钠溶液,生成沉淀的质量最大是
| A.2.9g | B.4.6g | C.5.5g | D.6.9g |