二甲氧苄胺嘧啶是一种用于家禽细菌感染防治药。其合成路线如下: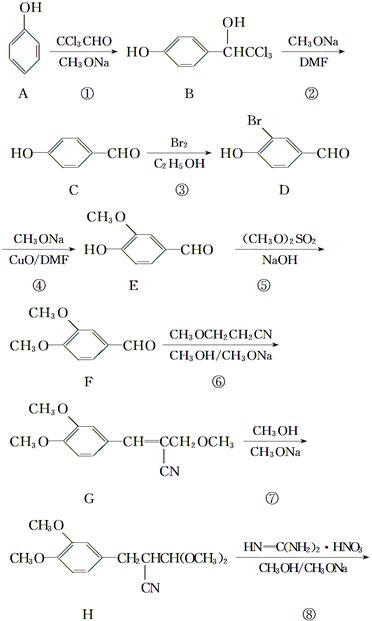
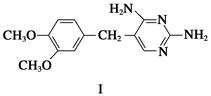
(1)化合物F的含氧官能团名称为________、__________;合成路线中,步骤①、④的反应类型分别为______________、____________。
(2)化合物B的核磁共振氢谱中有________个峰。
(3)写出F与新制氢氧化铜反应的化学方程式_______________________________。
(4)写出同时满足下列条件的E的同分异构体的结构简式:__________________________。
Ⅰ.分子中苯环上有两个取代基;
Ⅱ.能发生银镜反应;
Ⅲ.不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应;
Ⅳ.核磁共振氢谱显示有4个峰。
(5)实验生产的产品中存在一种结构为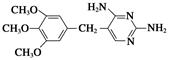 的副产物,为了使该产物的含量降到最低,需要合成路线中第________步反应的工艺最优化。
的副产物,为了使该产物的含量降到最低,需要合成路线中第________步反应的工艺最优化。
(6)已知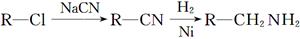 。化合物
。化合物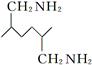 是合成染料的中间体,请写出以氯乙烷为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
是合成染料的中间体,请写出以氯乙烷为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
CH3CH2OH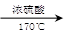 CH2=CH2
CH2=CH2 CH2—CH2
CH2—CH2
已知 X、Y、Z、Q、R、E六种元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如下表。
| 元素 |
结构或性质信息 |
| X |
原子的L层上s电子数等于p电子数。 |
| Y |
原子核外的L层有3个未成对电子。 |
| Z |
在元素周期表的各元素中电负性仅小于氟。 |
| Q |
单质常温、常压下是气体,原子的M层上有1个未成对的p电子。 |
| R |
核电荷数是Y与Q的核电荷数之和 |
| E |
原子序数比R大3 |
请根据信息回答有关问题:
(1)元素Y的原子核外共有 种不同运动状态的电子,有 种不同能级的电子。
(2)X、Y、Z三种元素的电负性由高到低的排列次序依次为(写元素符号) 。
(3)X、Z、Q元素均表现最低化合价时的三种氢化物中,沸点由高到低的排列次序依次为(写化学式) 。
(4)R的最高化合价为 。R的一种配合物的化学式为RCl3·6H2O。已知0.01 molRCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02 mol AgCl沉淀。此配合物最可能是 。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O
C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(5)元素E能形成八面体构型的配合物离子[E (YH3) x Q 2]+,则中心离子为(写化学式) ,配位体为(写化学式) ,x 的值为 。
(6)Y的最低价氢化物与Z的一种氢化物反应,生成的两种产物均不污染环境,其反应的化学方程式为 。
A~G是中学化学中常见的物质,在一定条件下它们之间的转化关系如图所示,其中A为金属,F是一种有毒的气体单质,G为NaOH溶液。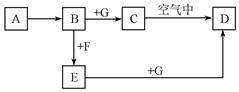
请回答问题。
(1)物质A的化学式是 。
(2)检验E溶液中的金属离子,常选用的试剂是 (填化学式)。
(3)溶液B与气体F反应的离子方程式是 。
(4)物质C转化为物质D的反应中伴随的主要现象是 ,化学方程式是 。
(5)将SO2气体通入BaCl2溶液中无沉淀产生,再将此溶液一分为二,向其中一份中通入足量的氨气,有白色沉淀产生,该沉淀是 (填化学式)。向另一份中滴加几滴E溶液也有白色沉淀产生,请用离子方程式表示该沉淀的产生过程 。
 从铝土矿(主要成分是
从铝土矿(主要成分是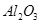 ,含
,含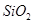 、
、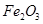 等杂质)中提取
等杂质)中提取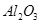 的两种方法如下:
的两种方法如下:
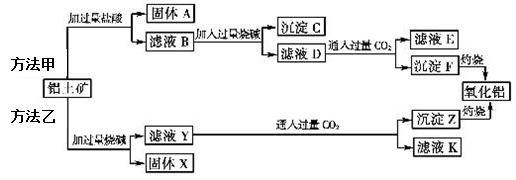
 请回答下列问题:
请回答下列问题: (1)方法甲中,固体A的化学式____________
(1)方法甲中,固体A的化学式____________ (2)方法乙加入烧碱后生成SiO32-的离子方程式为___________________
(2)方法乙加入烧碱后生成SiO32-的离子方程式为___________________ (3)简述检验滤液B中含
(3)简述检验滤液B中含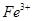 的方法______________________________
的方法______________________________ (4)滤液K中溶质的主要成份是 (填化学式),写出该物质的一种用途 。
(4)滤液K中溶质的主要成份是 (填化学式),写出该物质的一种用途 。
Ⅰ.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-。现进行如下实验:
a.取少量溶液,加入KSCN溶液,无明显变化
b.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色
c.向b中所得溶液中加入BaCl2溶液,有白色沉淀生成
d.向b中所得溶液中加入过量浓氨水,仅有红褪色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成
(已知Cu2+与过量浓氨水反应生成四氨合铜离子)请回答下列问题:
(1)该废水一定含有的离子是_____________;
(2)实验b中加入盐酸生成无色气体的离子方程式是________________;
(3)过滤除去d中的蓝色沉淀,调整溶液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为1:4,其离子方程式为Al+NO3-+OH- AlO2-+NH3+N2+H2O(未配平)。若除去0.2molNO3-,消耗铝___g。
AlO2-+NH3+N2+H2O(未配平)。若除去0.2molNO3-,消耗铝___g。
Ⅱ.某混合液中,可能大量含有的离子如下表:
| 阳离子 |
H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 |
Cl-、Br-、OH-、CO32-、AlO2- |
为探究其成分,某同学将Na2O2逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系分别如图所示:
(1)该溶液中一定含有的阳离子是_____________,溶液中一定不存在的阴离子是________。
(2)请写出沉淀减少的离子方程式________________________。
化合物A的分子式为C9H15OCl,分子中含有一个六元环和一个甲基,环上只有一个取代基;F分子中不含甲基:A与其它物质之间的转化如下图所示: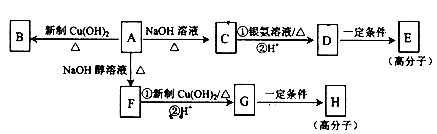
(1) A-F的反应类型是________________;G中含氧官能团的名称是____________。
(2)A-C的反应方程式是____________________。
(3)H的结构简式是____________________,E的结构简式是____________。
(4)有的同学认为B中可能没有氯原子,你的观点是________________(填“同意”或“不同意”)你的理由_______________。
(5)某烃的含氧衍生物X符合下列条件的同分异构体中,核磁共振氢谱显示为2组峰的是_____________(写结构简式);只含有两个甲基的同分异构体有____________种。
①相对分子质量比C少54;②氧原子数与C相同 ; ③能发生水解反应。