能正确表示下列反应的离子方程式是:( )
A.氯气通入水中,溶液呈酸性:Cl2+H2O  2H++Cl-+ClO- 2H++Cl-+ClO- |
| B.金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑ |
| C.向明矾溶液中滴加Ba(OH)2溶液,达沉淀物质的量最大:2Al3++3SO42-+3Ba2++6OH-=" 2" Al(OH)3↓+3BaSO4↓ |
| D.过量铁溶于稀硝酸:Fe+4H++NO3-=Fe3++NO↑+2H2O |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,1.12L1H2和0.2g2H2均含有0.1NA个质子 |
| B.在同压不同温的情况下,质量相同的O2和臭氧所含氧原子数不相同 |
| C.标准状况下,11.2L庚烷完全燃烧后生成的CO2分子数为3.5NA |
| D.常温下,将5.6 gFe投入足量的浓硫酸中转移电子数为0.3 NA |
下列解释事实的方程式不正确的是
A.向氯化铝溶液中滴加过量氨水,生成白色胶状沉淀:Al3++ 3NH3·H2O=Al(OH)3↓+ 3 |
| B.加入足量的氢氧化镁以除去氯化镁溶液中的少量氯化铁:Fe3+ + 3OH-=Fe(OH)3↓ |
C.常温下0.1mol/L 氯化铵溶液pH=5:NH4++H2O  NH3·H2O+ H+ NH3·H2O+ H+ |
| D.电解精炼铜时阳极铜溶解:Cu-2e-=Cu2+ |
工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为: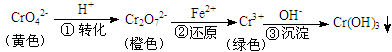
已知:步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)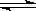 Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
下列有关说法不正确的是
A.步骤①中当v正(CrO42—) = 2v逆(Cr2O72—)时,说明反应:2CrO42—+2H+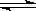 Cr2O72—+H2O 达到平衡状态 Cr2O72—+H2O 达到平衡状态 |
| B.若向K2Cr2O7溶液中加NaOH浓溶液,溶液可由橙色变黄色 |
| C.步骤②中,若要还原1 mol Cr2O72—离子,需要12 mol (NH4)2Fe(SO4)2 |
| D.步骤③中,当将溶液的pH 调节至5 时,可认为废水中的铬元素已基本除尽(当溶液中c(Cr3+) ≤10-5 mol/L时,可视作该离子沉淀完全) |
为实现下列实验目的,所用试剂合理的是
| 选项 |
实验目的 |
试剂 |
| A |
除去Fe2O3中的Al2O3 |
稀盐酸 |
| B |
验证Br2的氧化性强于I2 |
溴水、KI溶液、淀粉溶液 |
| C |
检验溴乙烷中含有溴元素 |
溴乙烷、NaOH溶液、AgNO3溶液 |
| D |
制备Fe(OH)3胶体 |
饱和FeCl3溶液、NaOH溶液 |
下列有关实验装置或实验操作正确的是