下列叙述中,正确的是( )
| A.氯化铝溶液中加入过量氨水反应实质是: Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| B.在加入铝粉能放出氢气的溶液中:K+、NH4+、CO32—、Cl-一定能够大量共存 |
| C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液 |
D.依据铝热反应原理,能发生反应:2Al+3MgO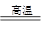 3Mg+Al2O3 3Mg+Al2O3 |
可逆反应①X(g)+2Y(g)
 2Z(g) 、②2M(g)
2Z(g) 、②2M(g) N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
下列判断正确的是
| A.反应①的正反应是吸热反应 |
| B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15 |
C.达平衡(I)时,X的转化率为 |
| D.在平衡(I)和平衡(II)中M的体积分数相等 |
已知反应:2CH3COCH3(l)  CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如下图所示。下列说法正确的是
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如下图所示。下列说法正确的是
| A.b代表0℃下CH3COCH3的Y-t曲线 |
B.反应进行到20min末,H3COCH3的 >1 >1 |
| C.升高温度可缩短反应达平衡的时间并能提高平衡转化率 |
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的 =1 =1 |
室温时,将浓度和体积分别为C1、V1的NaOH溶液和C2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是
| A.若PH>7,则一定是C1V1=C2V2 |
| B.在任何情况下都是C(Na+)+C(H+)=C(CH3COO-) +C(OH-) |
| C.当PH=7时,若V1=V2,一定是C2>C1 |
| D.若V1=V2,C1=C2,则C(CH3COO-) +C(CH3COOH)=C(Na+) |
向10mL 0.1mol·L−1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是
| A.x=10时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)>c(Al3+) |
| B.x=10时,溶液中有NH4+、AlO2-、SO42-,且c(NH4+)>c(SO42-) |
| C.x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)<c(AlO2-) |
| D.x=30时,溶液中有Ba2+、Al3+、OH-,且c(OH-) = c(Ba2+) |
下列叙述正确的是
| A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵 |
| B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小 |
| C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变 |
| D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |