控制适合的条件,将反应Fe3++Ag Fe2++Ag+设计成如图所示的原电池(盐桥装有琼脂—硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知接通后观察到电流计指针向右偏转。下列判断正确的是( )
Fe2++Ag+设计成如图所示的原电池(盐桥装有琼脂—硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知接通后观察到电流计指针向右偏转。下列判断正确的是( )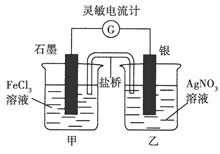
| A.在外电路中,电子从石墨电极流向银电极 |
| B.盐桥中的K+移向乙烧杯 |
| C.一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转 |
| D.电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转 |
用NA表示阿伏加罗常数,下列叙述正确的是
| A.标准状况下,22.4LCCl4含有的分子数为NA |
| B.2.3gNa与足量的氧气发生反应,转移的电子数为0.2NA |
| C.通常情况下,32gO2与32gO3所含有的氧原子数均为2NA |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-数目为NA |
下列分离与提纯的方法正确的是
| A.除去Mg粉中混有的Al粉:加入足量的氨水,过滤 |
| B.除去BaCO3固体中混有的BaSO4:加入过量盐酸后,过滤、洗涤 |
| C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| D.从I2的四氯化碳溶液中分离出I2:分液 |
下列关于Na2CO3与NaHCO3固体性质比较中,正确的是
| A.常温时,等浓度的溶液的碱性:Na2CO3<NaHCO3 |
| B.二者均可与澄清石灰水反应生成白色沉淀 |
| C.与同浓度的盐酸反应放出气体的速率快慢:Na2CO3>NaHCO3 |
| D.等质量的Na2CO3和NaHCO3分别与过量的盐酸反应,产物CO2的质量相等 |
下列离子方程式中,正确的是
| A.将Cl2通入H2O中:Cl2+H2O=2H++Cl-+ClO- |
| B.NaOH溶液中加入Al粉:2Al+4OH-=2AlO2-+2H2O |
| C.氯化亚铁溶液中加入新制氯水:Cl2+Fe2+═Fe3++2Cl- |
| D.NaHCO3溶液与盐酸的反应:HCO3-+H+=CO2↑+H2O |
下列溶液中氯离子数目与50mL1 mol•L-1的AlCl3溶液中氯离子数目相等的是
| A.150 mL 1mol/L的NaClO | B.150 mL 3 mol/L的KCl |
| C.75mL 2 mol/L的NH4Cl | D.5 mL 2 mol/L的CaCl2 |