下列离子方程式正确的是( )
| A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- |
| B.双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O |
C.用铜作电极电解CuSO4溶液:2Cu2++2H2O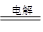 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| D.Na2S2O3溶液中加入稀硫酸:2S2O32—+4H+=SO32—+3S↓+2H2O |
已知 、
、 、
、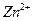 较完全地形成氢氧化物沉淀,溶液的pH分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量
较完全地形成氢氧化物沉淀,溶液的pH分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量 、
、 杂质离子,为除去这些离子制得纯净的硫酸锌,应加入的试剂是:
杂质离子,为除去这些离子制得纯净的硫酸锌,应加入的试剂是:
A.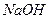 溶液 溶液 |
B. 、 、 |
| C.氨水 | D.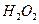 、 、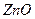 |
已知 溶液分别与
溶液分别与 溶液、
溶液、 溶液的反应情况如下:
溶液的反应情况如下:
(1) :
: (主要)
(主要) (次要)
(次要)
(2)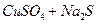 :
: (主要)
(主要) (次要)
(次要)
则下列对物质溶解度的比较正确的是:
A. |
B. |
C. |
D. |
下列各组离子,在指定的环境中一定能大量共存的是:
A.在由水电离出的 的溶液中: 的溶液中: 、 、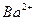 、 、 、 、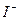 |
B.在加入铝粉能产生 的溶液中: 的溶液中: 、 、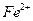 、 、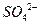 、 、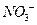 |
C.在能使pH试纸变深蓝色的溶液中: 、 、 、 、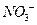 、 、 |
D.在pH为7的溶液中: 、 、 、 、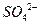 、 、 |
下列事实能说明氨水是弱电解质的是:
| A.氨水与氯化铝溶液反应产生氢氧化铝沉淀 |
| B.用氨水做导电实验,灯泡很暗 |
| C.0.1mol/L的氨水的pH<13 |
| D.氯化铵溶液的pH<7 |
物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是:
A.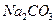 、 、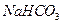 、 、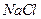 、 、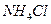 |
B.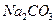 、 、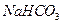 、 、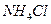 、 、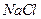 |
C.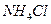 、 、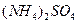 、 、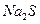 、 、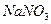 |
D.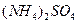 、 、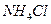 、 、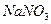 、 、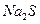 |