高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是( )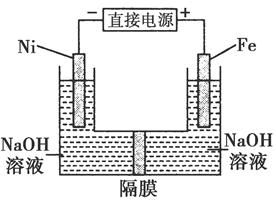
| A.铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+8H+ |
| B.镍电极上的电极反应为2H++2e-=H2↑ |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,最终溶液pH不变 |
下列说法正确的是( )
| A.非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 |
| B.只有非金属能形成含氧酸或含氧酸盐 |
| C.除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| D.非金属的最高价含氧酸都具有强氧化性 |
甲、乙为两种非金属元素,能说明甲比乙的非金属性强的是()
①甲比乙容易与H2化合 ②甲原子能与乙的阴离子发生置换反应③甲的最高价氧化物对应水化物的酸性比乙的最高价氧化物对应水化物的酸性强④与某金属反应时,甲原子得电子数目比乙的多⑤甲的单质熔沸点比乙的低
| A.只有④ | B.只有⑤ | C.①②③ | D.①②③④⑤ |
A、B、C、D、E是具有相同电子层数的1~18号元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D,E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是()
A.A、B、C、D、E B.E、C、D、B、A
C.B、A、D、C、E D.C、D、A、B、E
下列有关叙述正确的是()
| A.金属氧化物一定是碱性氧化物 | B.非金属氧化物一定是酸性氧化物 |
| C.碱性氧化物一定是金属氧化物 | D.酸性氧化物一定是非金属氧化物 |
下列各组粒子中,氧化性由强到弱、粒子半径由小到大的一组是()
| A.H+、Al3+、Mg2+、K+ |
| B.Na+、Mg2+、K+、Ca2+ |
| C.O、N、P、S |
| D.I、Br、Cl、F |