下列说法正确的是( )
| A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 |
| C.氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接存放在铝制容器中 |
| D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
下列说法中正确的是(NA表示阿伏加德罗常数的值)
| A.常温下,28g Fe与足量的浓硝酸反应,转移的电子数为1.5 NA |
| B.标准状况下,含4molHCl的浓盐酸与足量MnO2反应可生成22.4LCl2 |
| C.3.2 g铜在硫蒸气中完全燃烧,转移的电子数为0.1NA |
| D.常温常压下,0.1 mol氖气含有的电子数为NA |
关于元素周期表的说法正确的是
| A.第ⅠA族的元素都为金属元素 |
| B.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| C.过渡元素全部是金属元素 |
| D.周期表中有7个主族,7个副族,一个0族,一个VIII族,共16个族16个纵行 |
下列各物质中属于纯净物的是
①水玻璃 ②水泥 ③普通玻璃 ④漂白粉 ⑤Na2CO3·10H2O ⑥氯水 ⑦液氯 ⑧纯净的盐酸
| A.⑤⑦ | B.①⑤⑦⑧ | C.①⑤⑥ | D.①④ |
某密闭容器中充入等物质的量的气体A和B,一定温度下发生如下反应:A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化关系如图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化关系如图所示。下列说法中正确的是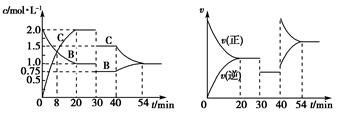
| A.反应方程式中的x=1, 30min时改变条件后,A的转化率将变减小 |
| B.前30 min内 A的反应速率为0.05 mol/(L·min) |
| C.20至40 min内表示处于平衡状态,该反应为放热反应 |
| D.30 min时改变的条件是加入负催化剂,40 min时改变的条件是升高温度 |
已知2SO2(g)+ O2(g) 2SO3(g)△H=-197 kJ·mol-1,向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g)△H=-197 kJ·mol-1,向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是
| A.容器内压强p:p甲=p丙<2p乙 |
| B.SO3的质量m:m甲=m丙<2m乙 |
| C.c(SO2)与c(O2)之比k:k甲=k丙>k乙 |
| D.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙 |