已知:A、B为单质,C为化合物, 。能实现该转化关系的是( )
。能实现该转化关系的是( )
①若C溶于水后得到强碱性溶液,则A可能是Na
②若C的溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C的溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.②④ C.①③ D.③④
下列说法中正确的是
A.AgCl悬浊液中存在平衡:AgCl(s)  Ag+(aq)+Cl-(aq),往其中加入少量NaCl固体,平衡向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq),往其中加入少量NaCl固体,平衡向左移动,溶液中离子的总浓度会减小 |
| B.AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI) |
| C.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 |
| D.硬水中含有较多的Ca2+、Mg2+、HCO3-、SO42-,加热煮沸可完全除去其中的Ca2+、Mg2+ |
反应N2(g)+3H2(g) 2NH3(g)△H<0在某一时间段中反应速率与反应过程的曲线关系如图,则图中氨的百分含量最低的时间段是
2NH3(g)△H<0在某一时间段中反应速率与反应过程的曲线关系如图,则图中氨的百分含量最低的时间段是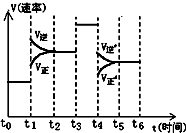
| A.t0-t1 | B.t2-t3 | C.t3-t4 | D.t5-t6 |
下列事实中不能证明CH3COOH是弱电解质的是
①常温下某CH3COONa溶液的pH=8②用CH3COOH溶液做导电实验,灯泡很暗③等pH等体积的盐酸、CH3COOH溶液和足量锌反应,CH3COOH放出的氢气较多④0.1mol/L的CH3COOH溶液的pH=2.1⑤pH=1的CH3COOH溶液稀释100倍,pH<3
| A.② | B.②⑤ | C.①③⑤ | D.③④⑤ |
在298 K、101.325 kPa时发生下列反应:①2H2(g)+O2(g)=2H2O(l) ②CaO(s)+CO2(g)=CaCO3(s);其熵变分别为ΔS1和ΔS2,则下列情况中正确的是
| A.ΔS1>0,ΔS2>0 | B.ΔS1<0,ΔS2<0 |
| C.ΔS1<0,ΔS2>0 | D.ΔS1>0,ΔS2<0 |
COCl2(g)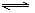 CO(g)+ Cl2(g) ΔH>0当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④扩大容积 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+ Cl2(g) ΔH>0当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④扩大容积 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |