四种短周期元素W、X、Y、Z的原子序数依次递增,X的一种单质能在空气中自燃。电解含有Y和Z的阴离子的混合溶液时,在阳极Y离子先失去电子。W和Z同主族。对于这四种元素下列判断正确的是( )
| A.气态氢化物的稳定性:W>X>Y>Z |
| B.单质的氧化性:W>Z>Y>X |
| C.四种元素原子半径大小:W<Y<Z<X |
| D.W单质可以将Z从其盐溶液中置换出来 |
某pH=1的X溶液中可能含有Fe2+、A13+、NH4+、CO32―、SO32―、SO42―、C1―中的若干种,现取X溶液进行连续实验,实验过程及产物如下: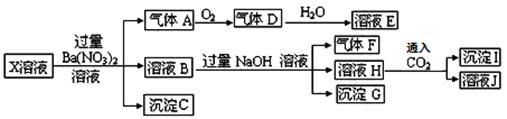
下列说法正确的是
| A.气体A是NO2 |
| B.X中肯定存在Fe2+、A13+、NH4+、SO42― |
| C.溶液E和气体F不能发生化学反应 |
| D.X中不能确定的离子是 A13+和C1― |
下图所示装置中,a、b都是惰性电极,通电一段时间后,a极附近溶液呈红色。下列说法正确的是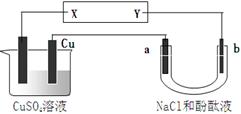
| A.NaCl溶液浓度不变 | B.X是负极,Y是正极 |
| C.CuSO4溶液浓度变小 | D.X是正极,Y是负极 |
常温常压下,乙烷、乙炔和丙烯组成的混合烃64mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了112 mL,原混合烃中乙炔的体积分数为
| A.12.5% | B.25% | C.50% | D.75 |
将34.2g C12H22O11(蔗糖)溶解在100 mL水中。关于所组成的溶液,下列叙述中正确的是
| A.该溶液中溶质的物质的量浓度为1 mol·L-1 |
B.该溶液溶质的质量分数为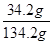 ×100% ×100% |
| C.该溶液中溶质的物质的量浓度的确定无需知道溶液的密度 |
| D.该溶液溶质的质量分数的确定还需知道溶液的密度 |
现在人类直接利用主要的化石能源是
| A.太阳能 | B.核能 | C.氢能 | D.煤 |