A、B、C、E、F为原子序数依次增大的六种元素,其中A、B、C、D、E为短周期元素,F为第四周期元素,F还是前四周期中电负极最小的元素。
已知:
A原子的核外电子数与电子层数相等;
B元素原子的核外p电子数比s电子数少1个;
C原子的第一至第四电离能为I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol;
D原子核外所有p轨道为全充满或半充满;
E元素的族序数与周期序数的差为4;
(1)写出E元素在周期表位置:________;D元素的原子的核外电子排布式:____________________。
(2)某同学根据题目信息和掌握的知识分析C的核外电子排布为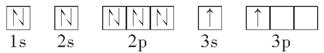
该同学所画的轨道式违背了________。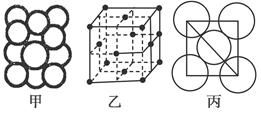
(3)已知BA5为离子化合物,写出其电子式:______________。
(4)DE3中心原子杂化方式为__________________,其空间构型为______________。
(5)某金属晶体中原子堆积方式如图甲,晶胞特征如图乙,原子相对位置关系如图丙,则晶胞中该原子配位数为________;空间利用率为________;该晶体的密度为________。(已知该金属相对原子质量为m,原子半径为a cm)
【2015海南化学】[选修5—有机化学基础]下列有机物的命名错误的是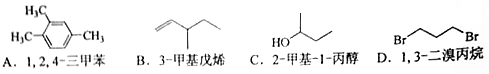
18—Ⅱ芳香族化合物A可进行如下转化: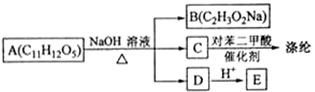
回答下列问题:
(1)B的化学名称为 。
(2)由C合成涤纶的化学方程式为 。
(3)E的苯环上一氯代物仅有两种,E的结构简式为 。
(4)写出A所有可能的结构简式 。
(5)写出符合下列条件的E的同分异构体的结构简式 。
①核磁共振氢谱显示苯环上仅有两种氢②可发生银镜反应和水解反应
【2015上海化学】(本题共12分)
局部麻醉药普鲁卡因E(结构简式为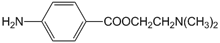 )的三条合成路线如下图所示(部分反应试剂和条件已省略):
)的三条合成路线如下图所示(部分反应试剂和条件已省略):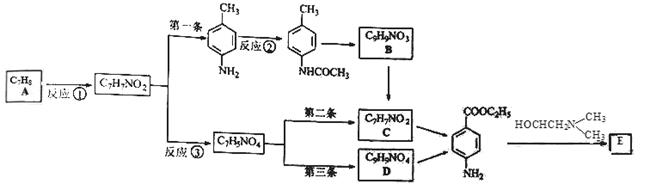
完成下列填空:
(1)比A多一个碳原子,且一溴代物只有3种的A的同系物的名称是 。
(2)写出反应试剂和反应条件。反应① ;③
(3)设计反应②的目的是 。
(4)B的结构简式为 ;C的名称是 。
(5)写出一种满足下列条件的D的同分异构体的结构简式。
①芳香族化合物
②能发生水解反应
③有3种不同环境的氢原子
1 mol该物质与NaOH溶液共热最多消耗 mol NaOH。
(6)普鲁卡因的三条合成路线中,第一条合成路线与第二条、第三条相比不太理想,理由是 。
【2015上海化学】(本题共10分)
对溴苯乙烯与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。
完成下列填空:
(1)写出该共聚物的结构简式
(2)实验室由乙苯制取对溴苯乙烯,需先经两步反应制得中间体 。
。
写出该两步反应所需的试剂及条件。
(3)将 与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色。
与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色。
A的结构简式为 。
由上述反应可推知 。
由A生成对溴苯乙烯的反应条件为 。
(4)丙烯催化二聚得到2,3-二甲基-1-丁烯,B与2,3-二甲基-1-丁烯互为同分异构体,且所有碳原子处于同一平面。
写出B的结构简式。
设计一条由2,3-二甲基-1-丁烯制备B的合成路线。
(合成路线常用的表示方式为: )
)
【2015江苏化学】化合物F是一种抗心肌缺血药物的中间体,可以通过以下方法合成:
(1)化合物A中的含氧官能团为_________和___________(填官能团的名称)。
(2)化合物B的结构简式为________;由C→D的反应类型是:_______。
(3)写出同时满足下列条件的E的一种同分异构体的结构简式_________。
Ⅰ.分子含有2个苯环 Ⅱ.分子中含有3种不同化学环境的氢
(4)已知: ,请写出以
,请写出以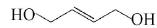 为原料制备化合物X(结构简式
为原料制备化合物X(结构简式 )的合成路线流程图(无机试剂可任选)。合成路线流程图示例如下:
)的合成路线流程图(无机试剂可任选)。合成路线流程图示例如下: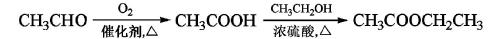
【2015广东理综化学】有机锌试剂(R—ZnBr)与酰氯(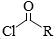 )偶联可用于制备药物Ⅱ:
)偶联可用于制备药物Ⅱ: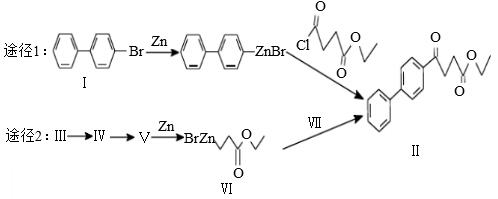
(1)化合物Ⅰ的分子式为 。
(2)关于化合物Ⅱ,下列说法正确的有 (双选)。
| A.可以发生水解反应 |
| B.可与新制的Cu(OH)2共热生成红色沉淀 |
| C.可与FeCl3溶液反应显紫色 |
| D.可与热的浓硝酸和浓硫酸混合液反应 |
(3)化合物Ⅲ含有3个碳原子,且可发生加聚反应,按照途径1合成线路的表示方式,完成途经2中由Ⅲ到Ⅴ的合成路线: (标明反应试剂,忽略反应条件)。
(4)化合物Ⅴ的核磁共振氢谱中峰的组数为 ,以H替代化合物Ⅵ中的ZnBr,所得化合物的羧酸类同分异构体共有 种(不考虑手性异构)。
(5)化合物Ⅵ和Ⅶ反应可直接得到Ⅱ,则化合物Ⅶ的结构简式为: 。