科学家根据元素周期律和原子结构理论预测,原子序数为114的元素位于第七周期第ⅣA族,称为类铅元素。下面关于它的原子结构和性质的预测正确的是( )
| A.类铅元素原子的最外层电子数为6 |
| B.其常见价态为+2、+3、+4 |
| C.它的金属性比铅强 |
| D.它的原子半径比铅小 |
【改编】对于常温下0.1 mol·L-1氨水和0.1 mol·L-1醋酸,下列说法正确的是
| A.0.1 mol·L-1醋酸溶液的pH<1 |
| B.0.1 mol·L-1醋酸溶液加水稀释,醋酸的电离程度增大,溶液中c(H+)和c(OH-)都减小 |
| C.若醋酸铵溶液显中性,则0.1 mol·L-1氨水和0.1 mol·L-1醋酸溶液中水的电离程度相同 |
| D.0.1 mol·L-1氨水与0.1 mol·L-1盐酸溶液等体积混合所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
镁—次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+ H2O + 2e-=Cl-+ 2OH-,关于该电池的叙述正确的是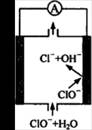
| A.该电池中镁为负极,发生还原反应 |
| B.电池工作时,OH-向正极移动 |
| C.电池工作时,正极周围溶液的pH将不断变小 |
| D.该电池的总反应为:Mg + ClO-+ H2O=Mg(OH)2↓+ Cl- |
【原创】用NA表示阿伏伽德罗常数的值。下列叙述正确的是
| A.50mL1mol/L葡萄糖溶液中所含分子数为0.05NA |
| B.常温下,0.2mol/LNa2CO3溶液中,含有阴离子的总数大于0.2NA |
| C.标准状况下,4.4gCO2与Na2O2完全反应,反应中转移的电子数为0.1NA |
| D.1 mol异丁烷中含有的共价键数为14NA |
【原创】下列各选项陈述I和陈述II均正确且二者有因果关系的是
| 陈述I |
陈述II |
|
| A |
常温下铁、铜均不溶于浓硝酸 |
常温下铁与浓硝酸发生钝化;铜与浓硝酸不反应 |
| B |
HCl与Na2SO3溶液反应生成SO2 |
用饱和Na2SO3溶液除去SO2中的少量HCl |
| C |
氨气液化时吸热 |
氨气常用作制冷剂 |
| D |
明矾和漂白粉常用于自来水的净化和杀菌消毒 |
两者的作用原理不同 |
【原创】在碱性溶液中能大量共存的离子组是
| A.Na+、K+、I-、ClO- |
| B.Ba2+、NH4+、Cl-、NO |
| C.K+、Na+、NO3-、S2— |
| D.Mg2+、K+、HCO3-、SO42- |