下列叙述中正确的是
| A.Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质 |
| B.蔗糖、油脂及它们的水解产物均为非电解质 |
| C.海水提取溴、煤的液化、焰色反应都发生了化学变化 |
| D.钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高 |
2005年1月,欧洲航天局的惠更斯号探测器首次成功登陆土星的最大卫星——土卫六。科学家对探测器发回的数据进行了分析,发现土卫六的大气层中含有95%的氮气,剩余的气体为甲烷和其他碳氢化合物。下列关于碳氢化合物的叙述正确的是()
| A.碳氢化合物的通式为CnH2n+2 | B.石油的主要成分是碳氢化合物 |
| C.乙炔是含碳量最高的碳氢化合物 | D.碳氢化合物中的化学键都是极性键 |
常温下将稀NaOH溶液和稀CH3COOH溶液混合,不可能出现的结果是()
| A.pH>7,且c(OH-)>c(Na+)> c(H+)>c(CH3COO-) |
| B.pH>7,且c(Na+)+c(H+)=c(CH3COO—)+c(OH-) |
| C.pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D.pH=7,且c(CH3COO-)>c(Na+)>c(H+)=c(OH-) |
下列离子方程式正确的是()
| A.碳酸氢钠溶液中加入盐酸 CO32- + 2H+ → CO2↑ + H2O |
| B.硫化亚铁与盐酸反应 S2- + 2H+ → H2S↑ |
| C.苯酚钠溶于醋酸溶液 C6H5O- + CH3COOH → C6H5OH + CH3COO- |
| D.氯化亚铁溶液中通入少量氯气 Fe2+ + Cl2 → Fe3+ + 2Cl- |
右图是某反应的微观示意图,“”、“”、“”分别表示质子数不同的3种原子。下列有关该反应的叙述正确的是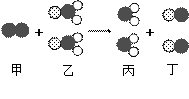

| A.乙中含有四种元素 |
| B.反应前后分子个数不变 |
| C.反应的本质是原子进行了重新组合 |
| D.甲、乙相对分子质量之和等于丙、丁相对分子质量之和 |
下列生产、生活中的做法正确的是
| A.将垃圾就地焚烧 | B.食用水果补充维生素 |
| C.随意丢弃塑料袋 | D.在牛奶中添加三聚氰胺 |