有机物H是一种合成药物的中间体,H的合成方案如下: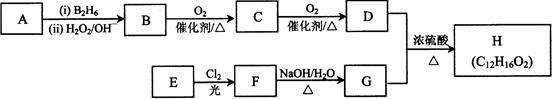
已知:R-CH=CH2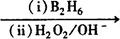 R-CH2-CH2OH
R-CH2-CH2OH
请回答下列问题:
(1)A是相对分子质量为104的芳香烃,A的分子式为 。
(2)鉴别A和C两种有机物试剂为 。
(3)F为一氯代物,其核磁共振氢谱有三个吸收峰,则E的结构简式为 。
(4)写出B→C的化学方程式: 。
(5)写出D和G生成H的化学方程式: 。
(6)D的同分异构体中能与FeCl3溶液发生显色反应且能发生银镜反应的有 种,写出其中核碰共振氢谱中吸收峰数目最少的结构简式:_____________。
某无色透明溶液中可能大量存在Ba2+、Mg2+、Fe3+中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是。
(2)取少量原溶液加入过量稀硫酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定有的离子,有关的离子反应式为。
(3)取(2)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有。
(4)原溶液中可能大量存在的阴离子是下列A~C中的(填序号)。
A.OH-B.NO3-C.CO32-
用98%的浓H2SO4(ρ=1.84g/cm3)配制500ml0.5mol/L的稀H2SO4,请按要求填空:
⑴所需浓H2SO4的体积为
⑵如果实验室有10mL、20mL、50mL量筒,应选用 mL量筒,实验中还需要用到的仪器有
⑶若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷至室温即进行定容
②定容时俯视刻度线
⑷若定容时液面高于刻度线应采取的措施是
把氯气(Cl2)通入水中,氯气与水反应生成盐酸和次氯酸(HClO)。次氯酸是一种强氧化剂,能杀死水中的细菌。所以自来水厂常用氯气来杀菌消毒。请仔细阅读上述信息,回答下列问题。
(1)写出氯气与水反应的化学方程式:。
(2)次氯酸中氯元素的化合价是。
(3)不法商贩常用自来水假冒矿泉水或纯净水出售,坑害消费者。请你设计一个简单的实验,来识别用自来水假冒的矿泉水或纯净水。(简述操作步骤、现象和结论)
选择下列实验方法分离物质,将分离方法的序号填在横线上。
| A.萃取分液 | B.升华 | C.结晶 | D.分液 E.蒸馏 F.层 析 G.过滤 |
(1)______分离饱和食盐水与沙子的混合物。
(2)______从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)______分离水和汽油的混合物。
(4)______分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
人造空气(氧气和氦气的混合气体)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,5.6 L“人造空气”的质量是2.4 g,其中氧气与氦气和体积比是______ ,氧气的质量是______。