下列有关溶液中微粒的物质的量浓度关系正确的是
A.某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)=c(H+)+c(H2A)
B.0.1 mol·L-1CH3COONa 溶液与0.05 mol·L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)> c(CH3COOH) > c(Cl-) >c(H+)
C.物质的量浓度相等的HCN溶液和NaCN溶液等体积混合后的溶液中:c(CN-)+2c(OH-)=2c(H+)+c(HCN)
D.0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3·H2O)+c(Fe2+)=0.3 mol·L-1
乳糖是一种二糖,可以水解生成葡萄糖和半乳糖。半乳糖和葡萄糖互为同分异构体,则乳糖的分子式为( )
| A.C6H12O6 |
| B.C18H30O15 |
| C.C12H24O12 |
| D.C12O22O11 |
某期刊封面上有如下图所示的一个分子的球棍模型图。图中:“棍”代表单键或双键;
不同颜色的球代表不同元素的原子。该模型图可代表一种( )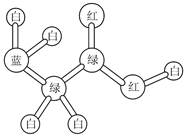
| A.卤代羧酸 | B.酯 | C.氨基酸 | D.醇钠 |
有A、B两种烃,含碳元素的质量分数相等,下列关于A和B的叙述正确的是( )
A.A和B一定是同分异构体
B.A和B不可能是同系物
C.A和B实验式一定相同
D.A和B各1 mol完全燃烧后生成的CO2的质量一定相等
下列各组物质属于同分异构体的是()


①已知乙烯可被KMnO4溶液氧化。
②乙醇能在一定条件下发生脱水反应。
今以 为原料通过下列反应来制取有机玻璃:
为原料通过下列反应来制取有机玻璃:


(1)请填出上面方框内的有机物的结构简式。
(2)写出反应①和反应②的化学方程式:
反应①:__________________________________________________;
反应②:__________________________________________________。