如下图所示的两个实验装置,溶液的体积均为200mL。开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液的体积变化,下列叙述中正确的是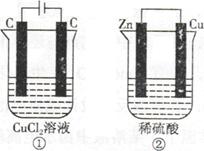
| A.产生气体的体积:①>② |
| B.溶液的pH变化:①减小,②增大 |
| C.电极上生成物质的质量:①=② |
| D.电极反应式:①中阳极2Cl—-2e—=Cl2↑,②中负极2H++2e—=H2↑ |
对处于化学平衡的体系,以化学平衡与化学反应速率的关系可知
| A.化学反应速率变化时,化学平衡一定发生移动。 |
| B.化学平衡发生移动时、化学反应速率一定变化。 |
| C.正反应进行的程度大、正反应速率一定大。 |
| D.只有催化剂存在下,才会发生化学反应速率变化,而化学平衡不移动的情况。 |
等质量的钠、镁、铝分别与足量盐酸反应,产生H2的质量由大到小排列顺序正确的
| A.Al、Mg、Na | B.Mg、Al、Na | C.Na、Mg、Al | D.Na、Al、Mg |
某溶液中有Mg2+、Fe2+、Fe3+和Al3+四种阳离子,若向其中加入过量的NaOH溶液,微热并搅拌,过滤,再在滤渣中加入过量的盐酸,所得溶液中大量增加的阳离子是
| A.Mg2+ | B.Al3+ | C.Fe2+ | D.Fe3+ |
向HCl酸化的AlCl3溶液中逐滴滴入NaOH溶液,图中能正确表示这个反应的是
(纵坐标表示生成沉淀的质量,横坐标表示加入NaOH溶液的体积)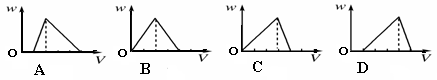
能在水溶液中大量共存的一组离子是
| A.Fe2+、Fe3+、Na+、NO3- | B.Fe3+、NH4+、SCN−、Cl− |
| C.H+、I−、Na+、SiO32- | D.NH4+、OH-、Cl-、SO32- |