化学与生产和生活密切相关,下列说法不正确的是
| A.温室效应导致海水的酸度增加,珊瑚、贝壳类等生物的生存将会受到威胁 |
| B.焰火的五彩缤纷是某些金属元素的性质的展现 |
| C.对“地沟油”进行分馏可得到汽油 |
| D.将煤气化后再作为能源,可以减少PM2.5引起的危害 |
向CH3COOH+C2H5OH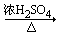 CH3COOC2H5+H2O的平衡体系中加入
CH3COOC2H5+H2O的平衡体系中加入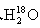 ,过段时间后
,过段时间后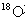 在有机物中
在有机物中
| A.只存在于乙酸分子中 | B.只存在于乙醇分子中 |
| C.只存在于乙醇、乙酸乙酯分子中 | D.乙酸乙酯、乙酸分子中 |
实验室用乙酸、乙醇、浓H2SO4制取乙酸乙酯,加热蒸馏后,在饱和Na2CO3溶液的上面得到无色油状液体,当振荡混合时,有气泡产生,原因是
| A.产品中有被蒸馏出的H2SO4 | B.有部分未反应的乙醇被蒸馏出来 |
| C.有部分未反应的乙酸被蒸馏出来 | D.有部分乙醇跟浓H2SO4作用生成乙烯 |
某种有机物的氧化产物是甲,还原产物是乙.甲和乙都能与钠反应放出氢气.甲和乙反应生成丙.甲和丙都能发生银镜反应.则该有机物是
| A.甲醇 | B.甲醛 | C.甲酸 | D.乙醛 |
可用来鉴别甲酸与乙酸的方法是
| A.用石蕊试液加以鉴别 | B.加入乙醇及浓硫酸加热 |
| C.用碱中和后加入银氨溶液用水浴加热 | D.加入氢氧化钠溶液鉴别 |
以下化合物中能使溴水褪色,也能发生聚合反应和酯化反应的是
| A.CH2=CH—CHO | B.CH3—CH2—CH2OH |
| C.CH2=CH—COOH | D.C6H5—CH2—COOH |