室温下,用0.100 mol/L NaOH 溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,
下列说法正确的是
| A.起始时盐酸和醋酸溶液PH相同 |
B.V(NaOH)="10.00" mL 时, <1 <1 |
| C.pH=7时,两种酸所用NaOH溶液体积不相等,醋酸用的体积多 |
| D.V(NaOH)="20" .00 mL 时,c(Cl‾)>c(CH3COO—) |
300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol/L Ba(OH)2溶液300 mL,反应后溶液中SO42-的物质的量浓度约为
| A.0.4 mol/L | B.0.3 mol/L |
| C.0.2 mol/L | D.0.1 mol/L |
同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是
| A.密度比为16∶11 |
| B.分子个数比为16∶11 |
| C.体积比为1∶1 |
| D.氧原子个数比为1∶1 |
a g NH3含b个氢原子,则阿伏加德罗常数可表示为
A.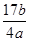 |
B.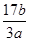 |
C.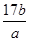 |
D.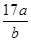 |
下列说法中正确的是
| A.将322 g Na2SO4·10H2O溶于1 L水中,所得溶液的物质的量浓度为1 mol·L-1 |
| B.将1 L 2 mol·L-1 H2SO4溶液加水稀释到2 L,所得溶液的物质的量浓度为1 mol·L-1 |
| C.将1 L 18.4 mol·L-1的H2SO4溶液加入到1 L水中,所得溶液的物质的量浓度为9.2 mol·L-1 |
| D.将336 mL HCl气体溶于水,配成300 mL溶液,所得溶液的物质的量浓度为0.05 mol·L-1 |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.32 g O2所含的原子数目为NA |
| B.0.5 mol H2SO4含有的原子数目为3.5NA |
| C.HNO3的摩尔质量是63 g |
| D.0.5NA个氯气(Cl2)分子的物质的量是1 mol |