我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是( )
| A.正极反应式为O2+2H2O+4e-=4OH- |
| B.电池工作时,电流由铝电极沿导线流向铂电极 |
| C.以网状的铂为正极,可增大与氧气的接触面积 |
| D.该电池通常只需要换铝板就可以继续使用 |
为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,下列物质中最好选用 ( )
| A.H2O2溶液 | B.KMnO4溶液 | C.Cl2水 | D.HNO3溶液 |
下列叙述正确的是( )
| A.Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物 |
| B.Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀 |
| C.NaCl与Na2CO3灼烧时火焰颜色不相同 |
| D.Na2O2可作供氧剂,而Na2O不行 |
将一定量铁粉和铜粉的混合物加入由稀硫酸和稀硝酸组成的混合溶液中,充分反应后金属粉末有剩余,下列有关推断正确的是
| A.反应过程中不可能产生H2 |
| B.剩余的金属粉末一定有铜 |
| C.往反应后的溶液中加入KSCN溶液会变血红色 |
| D.往反应后的溶液中加入足量的稀H2SO4,则金属粉末的质量一定会减少 |
在T℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含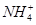 的物质的量为b mol。下列叙述中正确的是( )
的物质的量为b mol。下列叙述中正确的是( )
A.溶质的质量分数为w= ×100% ×100% |
| B.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
C.溶液中c(OH-)=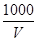 mol·L-1 mol·L-1 |
D.溶质的物质的量浓度c= mol·L-1 mol·L-1 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是()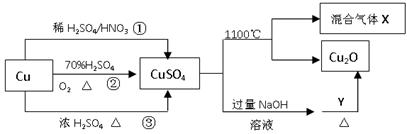
| A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 |
| B.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| C.1molCuSO4在1100℃所得混合气体X中O2可能为0.75mol |
| D.Y可以是葡萄糖 |