下列物质中,既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
①SO2 ②CH3CH2CH=CH2 ③ ④CH3CH3
④CH3CH3
| A.①②③④ | B.③④ |
| C.①②④ | D.①② |
下列分散系中的分散质的粒子大小属于纳米级(1~100 nm)的是()
| A.Fe(OH)3胶体 | B.Fe(OH)3沉淀 |
| C.FeCl3溶液 | D.碘水与CCl4溶液振荡后的混合液 |
标况下,下列物质中体积最大的是 ( )
| A.22.4 L H2 | B.含3.01×1023个分子的Cl2 |
| C.10g NH3 | D.0.8 mol CO2 |
等质量的下列物质所含分子数最多的是( )
| A.H2 | B.O2 | C.N2 | D.CO2 |
嫦娥一号探月卫星的任务之一是对月球上的氦-3(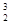 He)分布情况进行探测。
He)分布情况进行探测。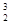 He表示的氦原子( )
He表示的氦原子( )
| A.核外电子数为3 | B.质量数为3 |
| C.核内中子数为3 | D.核内质子数为3 |
下列物质中,属于电解质的是( )
| A.氧气 | B.铜 | C.蔗糖(C12H22O11) | D.碳酸氢钠 |