碳及其化合物应用广泛。
I.工业上利用CO和水蒸汽反应制氢气,存在以下平衡:CO(g)+H2O(g) 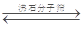 CO2(g)+H2(g)
CO2(g)+H2(g)
(1)沸石分子筛中含有硅元素,请写出硅原子结构示意图__________。
(2)向1L恒容密闭容器中注人CO和H2o(g),830℃时测得部分数据如下表。则该温度下反应的平衡常
数K=______________。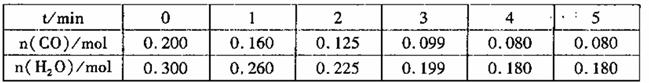
(3)相同条件下,向1L恒容密闭容器中,同时注人1mol CO、1mol H2O(g),2molCO2和2mo1 H2,此时v(正 ) __________v(逆)(填“>”“=”或“<”)
II.已知CO(g)+1/2 O2 (g)=CO2 (g) △H=一141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g) △H=一484 kJ·mol-1
CH3OH(1)+3/2O2 (g)=CO2(g)+2H2O(g) △Hl=一726 kJ·mol-1
(4)利用CO、H2化合制得液态甲醇的热化学方程式为___________。
III.一种新型氢氧燃料电池工作原理如下图所示
(5)写出电极A的电极反应式_____________。
(6)以上述电池电解饱和食盐水,若生成0.2mo1 Cl2,则至少需通人O2的体积为_____L(标准状况)。
20.(12分)ZnMnO2干电池应用广泛,其电解质溶液是ZnCl2—NH4Cl混合溶液。
(1)该电池的负极材料是________。电池工作时,电子流向________(填“正极”或“负极”)。
(2)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是__________________。
欲除去Cu2+,最好选用下列试剂中的________(填代号)。
a.NaOHb.Znc.Fed.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是_________ ___。若电解电路中通过2 mol电子,MnO2的理论产量为________g。
19.下表是不同温度下水的离子积数据:
| 温度 / ℃ |
25 |
t1 |
t2 |
| 水的离子积常数 |
1×10-14 |
α |
1×10-12 |
试回答下列问题:
(1)若25<t1<t2,则α________1×10-14(填“>”“<”或“=”),作出此判断的理由是____________。
(2)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol·L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=________
(3)t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=____________。此溶液中各种离子的浓度由大到小的排列顺序是____________________。
18.(12分)在一恒温恒容体积为1 L的容器中存在如下可逆反应:2NO2(g) 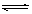 N2O4(g),已知NO2、N2O4的消耗速率与本身浓度存在下列关系v(NO2) = k1·c(NO2)2,v(N2O4) = k2·c(N2O4)其中k1、k2反应及温度有关的常数,可以根据上述关系式建立一个速率-浓度的图像如下
N2O4(g),已知NO2、N2O4的消耗速率与本身浓度存在下列关系v(NO2) = k1·c(NO2)2,v(N2O4) = k2·c(N2O4)其中k1、k2反应及温度有关的常数,可以根据上述关系式建立一个速率-浓度的图像如下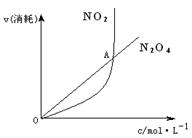
试回答下列问题
(1)图中的交点A对应该可逆反应的状态是否达到化学平衡状态?_填“是”或“否”)作出判断的理由是_________________
(2)若k1= k2,则在开始时向该容器中充入1molNO2,则达到平衡时NO2的浓度为____mol·L-1,N2O4的浓度为___mol·L-1
(3)若k1≠k2,则在开始时向该容器中充入1 molNO2,设达到平衡时NO2的浓度为c1,N2O4的浓度为c2,则c1与c2的关系为,c1、c2、k1、k2存在的关系为______
⑵(12分) 18℃时,H2A(酸):K1=4.3×10-7,K2=2.1×10-12。H2B(酸):K1=1.0×10-7,K2=6.3×10-13,在浓度相同的两种溶液中,用“>”、“<”或“=”填空。
①H+的浓度:H2A________H2B;
②酸根离子的浓度:c (A2-)________c (B2-);
③酸分子的浓度:c (H2A)________c (H2B);
④溶液的导电能力:H2A________H2B。
17.⑴(9分)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
①请写出方框内物质的化学式:。
②针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是的影响。
③若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是。
| A.硫酸钾 | B.硫酸锰 | C.水 | D.氯化锰 |