镭是元素周期表中第7周期第ⅡA族元素,关于其叙述不正确的是( )。
| A.镭的金属性比钙弱 |
| B.单质能与水反应生成H2 |
| C.镭在化合物中呈+2价 |
| D.碳酸镭难溶于水 |
下图是部分短周期主族元素原子半径与原子序数的关系图,下列说法正确的是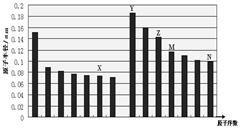
| A.最高价含氧酸的酸性:M>N |
| B.离子半径:X<Y |
| C.X和Y形成的化合物中一定含有含离子键 |
| D.化合物MX2能与碱反应,不能与任何酸反应 |
我国稀土资源丰富。下列有关稀土元素144 62Sm与150 62Sm的说法正确的是()
| A.144 62Sm与150 62Sm互为同位素 | B.144 62Sm与150 62Sm 的质量数相同 |
| C.144 62Sm与150 62Sm是同一种核素 | D.144 62Sm与150 62Sm的核外电子数和中子数均为62 |
设nA 为阿伏加德罗常数的数值 ,下列说法正确的是(相对原子质量:O-16)
| A.常温下,8gO2和O3的混合气体中含有4nA个电子 |
| B.1molFe2+与足量的H2O2溶液反应,转移2nA个电子 |
| C.1 L 0.1 mol ·L-1NaHCO3液含有0.1nA个HCO3- |
| D.常温常压下,22.4L的NO2 和CO2混合气体含有2 nA个氧原子 |
氯气是一种重要的工业原料。工业上利用反应在3Cl2+8NH3=N2+6NH4Cl检查氯气管道是否漏气。下列说法正确的是
| A.若管道漏气遇氨就会产生白雾 | B.该反应利用了氨气的还原性 |
| C.该反应属于复分解反应 | D.生成6molNH4Cl有18mol电子转移 |
下列陈述I、II正确且有因果关系的是
| 选项 |
陈述I |
陈述II |
| A |
SO2有漂白性 |
SO2可使酸性高锰酸钾溶液褪色 |
| B |
硫酸铜是强酸弱碱盐 |
蒸干CuSO4溶液可以得到Cu(OH)2固体 |
| C |
SO2是酸性氧化物 |
将SO2通入BaCl2溶液可生成BaSO3沉淀 |
| D |
氢氧化铝显两性 |
向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaOH溶液,沉淀消失 |