下列叙述错误的是( )。
| A.带相反电荷的离子之间的相互吸引力称为离子键 |
| B.金属元素与非金属元素化合时,不一定形成离子键 |
| C.某元素的原子最外层只有一个电子,它与卤素结合时所形成的化学键不一定是离子键 |
| D.非金属元素也可能形成离子键 |
分类是化学学习和研究中的常有用手段,下列分类依据和验论都正确的是
| A.浓HC1、浓H2SO4、浓HNO3均具有氧化性,都属氧化性酸 |
| B.Na2O、SO2、BaSO4在熔融状态或溶于水时均能导电,都属电解质 |
| C.NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物 |
| D.金刚石、二氧化硅、碳化硅晶体中的原子均能以共价键结合,都属原子晶体 |
下列说法中,正确的是
| A.石油是由液态烷烃、烯烃和少量芳香烃组成的混合物 |
| B.40%的甲醇水溶液称成为福尔马林,常用于浸制生物标本 |
| C.乙醇、乙烯、乙醛都能使酸性高锰酸钾溶液褪色 |
| D.油脂、淀粉水解都生成甘油 |
工业上用CO和H2合成CH3OH:CO(g)+2H2(g) CH3OH(g)。反应的平衡常数如下表:
CH3OH(g)。反应的平衡常数如下表:
| 温度/℃ |
0 |
100 |
200 |
300 |
400 |
| 平衡常数 |
667 |
13 |
1.9×10-2 |
2.4×10-4 |
1×10-5 |
下列说法正确的是
A.该反应的△H> 0
B.加压、增大H2浓度和加入催化剂都能提高CO的转化率
C.工业上采用5 ×103 kPa和250℃的条件,其原因是原料气的转化率高
D.t℃时,向1 L密闭容器中投入0.1 mol CO和0.2 mol H2,平衡时CO转化率为50%,则该温度时反应的平衡常数的数值为100
下述实验方案能达到实验目的的是
| 编号 |
A |
B |
C |
D |
| 实验 方案 |
 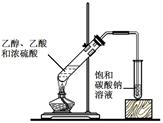 |
 |
 |
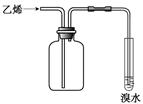 |
| 实验 目的 |
实验室制备乙酸乙酯 |
分离乙酸和水 |
验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 |
收集乙烯并验证它与溴水发生加成反应 |
工业上常用氯氧化法处理含氰(CN-)废水,一定条件下,氯气和CN-反应生成无毒气体。下列说法不正确的是
| A.CN-中碳元素的化合价为+2 |
| B.该反应的产物之一是无毒的N2 |
| C.当1 molCN-参与反应时,转移3 mol e- |
| D.处理含0.1 mol CN-的废水,理论上需要消耗标准状况下Cl2的体积为5.6L |