根据下列事实:①A+B2+=A2++B;②D+2H2O=D(OH)2+H2↑;③以B、E为电极与E的盐溶液组成原电池,电极反应为E2++2e-=E,B-2e-=B2+,由此可知A2+、B2+、D2+、E2+的氧化性强弱关系是________。
生活处处有化学。下列说法正确的是
| A.利用60Co的放射性可治疗某些疾病。60Co和59Co互为同位素 |
| B.明矾净水和 “84” 消毒液消毒的原理相同 |
| C.碳酸钡、硫酸钡等难溶性钡盐均可用于钡餐透视 |
| D.月饼包装盒中常放入铁粉作干燥剂 |
在2 L的密闭容器中进行如下反应: CO(g)+H2O(g) CO2(g)+H2(g),有如下数据:
CO2(g)+H2(g),有如下数据:
| 实验 |
温度/℃ |
起始量/mol |
平衡量/mol |
|||
| CO |
H2O |
CO2 |
H2 |
CO2 |
||
| 1 |
650 |
2.0 |
1.0 |
0 |
0 |
0.8 |
| 2 |
800 |
2.0 |
2.0 |
0 |
0 |
1.0 |
下列说法正确的是
A.正反应为吸热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K=8/3
D.实验1再加入1.0 mol H2O,重新达到平衡时,n (CO2)为1.6 mol
有25℃时0.1 mol/L的①氯化铵、②氯化钠、③醋酸钠三种溶液。下列有关判断不正确的是
| A.①与②比较:c(Na+)>c(NH4+) |
| B.①中离子浓度的大小关系是:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C.①和②等体积混合的溶液中:c(Cl-)=c(Na+)+c(NH4+)+c(NH3·H2O) |
| D.向③中滴加适量醋酸溶液,使溶液pH=7,则:c(CH3COO-)>c(Na+) |
利用下列装置分别完成相关实验,不能达到实验目的的是
| A |
B |
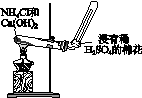 制备并收集氨气 |
 验证铁的吸氧腐蚀 |
| C |
D |
 鉴别碳酸钠与碳酸氢钠 |
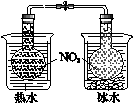 证明温度对平衡移动的影响 |
已知:Li与Mg、Be与Al的性质相似。下列判断正确的是
| A.LiOH是强碱 |
| B.Be与冷水剧烈反应 |
| C.Li在空气中不易被氧化 |
| D.Be(OH)2能与NaOH溶液反应 |