X、Y、Z、W是前20号元素,原子序数依次增大。X是原子半径最小的元素;Y元素原子的最外层电子数是电子层数的2倍;Z元素的-1价阴离子的核外电子排布与氖原子相同,W元素为金属,它的某种化合物可用于烟气脱硫。下列说法错误的是
| A.X、Y形成的化合物中可能含有双键 |
| B.X单质和Z单质在暗处能剧烈反应 |
C.W元素与Z元素形成的化合物用电子式表示形成过程为: |
| D.XZ的沸点在与Z同族的其它X的化合物中最高 |
2007年4月27—29日,在上海召开第八届中国国际环保展览会。上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于
| A.无机物 | B.有机物 | C.盐类 | D.非金属单质 |
将铜粉放入稀硫酸中,加热无明显现象发生。但加入某盐后,发现铜粉质量逐渐减少,该盐可能是
| A.Fe2(SO4)3 | B.ZnSO4 | C.KNO3 | D.NaCl |
下列离子方程式正确的是
A.硫酸镁溶液跟氢氧化钡溶液反应: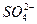 +Ba2+====BaSO4↓ +Ba2+====BaSO4↓ |
B.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++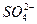 ====BaSO4↓+2H2O ====BaSO4↓+2H2O |
| C.铜片插入硝酸银溶液中:Cu+2Ag+====Cu2++2Ag |
| D.澄清石灰水中加入盐酸Ca(OH)2+2H+====Ca2++2H2O |
下列对“摩尔(mol)”的叙述不正确的是
| A.摩尔是一个单位,用于计量物质所含微观粒子的多少 |
| B.摩尔既能用来计量纯净物,又能用来计量混合物 |
| C.1 mol任何气体所含的气体分子数目都相等 |
| D.用“摩尔”(而不用“个”)计量微观粒子与用“纳米”(而不用“米”)计量原子直径,计量思路都是扩大单位 |
浊液区别于其他分散系最本质的特征是
| A.外观浑浊不清 |
| B.浊液没有丁达尔现象 |
| C.不稳定 |
| D.分散质粒子直径大于100 nm |