下列指定分散系中能大量共存的微粒是
| A.空气: CH4、CO2、SO2、NO |
| B.银氨溶液: Na+、H+、NO3-、NH4+ |
| C.pH=2的溶液: H+、K+、Cl-、Br- |
| D.高锰酸钾溶液: H+、Na+、SO42-、HCOOH |
同温同压下,等质量SO2和CO2相比较,下列叙述中正确的是
| A.密度比为16∶11 | B.密度比为11∶16 |
| C.体积比为1∶1 | D.体积比为16∶11 |
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:
Fe3+→Fe2+;MnO4-→Mn2+ ;IO3-→ I2;HNO3→NO
I2;HNO3→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
| A.Fe3+ | B.MnO4- | C.IO3- | D.HNO3 |
下列离子方程式正确的是
| A.过氧化钠与水反应: 2O22-+2H2O==O2↑+4OH- |
| B.次氯酸钠与Fe(OH)3在碱性溶液中反应生成Na2FeO4: 3ClO-+2Fe(OH)3==2FeO42-+3Cl-+H2O+4H+ |
| C.向明矾[KAl(SO4)2·12H2O]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀: 2Al3++3SO42-+3Ba2++6OH-==2Al(OH)3↓+3BaSO4↓ |
| D.向碳酸氢镁溶液中加入过量的澄清石灰水: |
Mg2++2HCO3-+2Ca2++4OH-==Mg(OH)2↓+2CaCO3↓+2H2O
在VmlAl2(SO4)3溶液中含有Al3+mg,取V/4ml该溶液用水稀释至4Vml,则SO42-物质的量浓度为
A.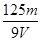 mol/L mol/L |
B.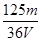 mol/L mol/L |
C.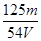 mol/L mol/L |
D.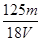 mol/L mol/L |
有下列三个反应:①C12+FeI2 = FeC12+I2②2Fe2++Br2 = 2Fe3++2Br-
③Co2O3+6HC1 = 2CoC12 + Cl2↑+3H2O,下列说法正确的是
| A.①②③中氧化产物分别是FeC12、Fe3+、C12 |
| B.根据以上方程式可以得到氧化性C12>Co2O3>Fe3+ |
| C.在反应③中生成1molCl2时,有2molHC1被氧化 |
| D.根据反应①②一定可以推理得到C12+FeBr2 = FeC12+Br2 |