下列离子方程式的书写及评价均合理的是
| 选项 |
离子方程式 |
评价 |
| A |
将1molCl2通入到含1molFeI2的溶液中: 2Fe2++2I-+2Cl2 =2Fe3++4Cl-+I2 |
正确;Cl2过量,可将 Fe2+ 、I-均氧化 |
| B |
Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2++ HCO3-+ OH-=MgCO3↓+ H2O |
正确;酸式盐与碱反应 生成正盐和水 |
| C |
过量SO2通入到NaClO溶液中: SO2 + H2O + ClO-= HClO+HSO3- |
正确;说明酸性: H2SO3强于HClO |
| D |
1mol/L的Na [Al(OH)4]溶液和2.5mol/L的HCl溶 液等体积互相均匀混合:2[Al(OH)4]-+ 5H+ = Al3+ +Al(OH)3↓+ 5H2O |
正确;[Al(OH)4]-与 Al(OH)3消耗的H+的物 质的量之比为2:3 |
俄罗斯科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的一种核素为 。下列有关叙述正确的是( D )
。下列有关叙述正确的是( D )
A.X元素的核外电子数为288
B.核素 的质量数与中子数之差为173
的质量数与中子数之差为173
C.113号元素属于非金属元素
D.115号元素的最高正化合价是 +5
随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。下列有关说法中,正确的是
| A.N5+离子中含有36个电子 | B.C60的摩尔质量为720g |
| C.H2和H3属于同素异形体 | D.O2和O4属于同位素 |
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核才有NMR现象。试判断下列哪组原子均可产生NMR现象()
| A.18O、31P、119Sn | B.27Al、19F、12C |
| C.7N、15P、33As、51Sb、83Bi | D.只有一个电子层的原子 |
下列说法正确的是()
A.我国最近合成的一种新核素 ,该核素形成的最高价氧化物的水化物的相对分子质量为98 ,该核素形成的最高价氧化物的水化物的相对分子质量为98 |
| B.某元素的一种核素X失去两个电子,电子数为a ,中子数为b,该元素的相对原子质量约为a+2+b |
C.活泼金属元素R有某种同位素的氯化物RClX,该氯化物中R微粒核内中子数为Y,核外电子数为Z,该核素可以表示为 |
| D.某元素的一种核素X的质量数是A,含有N个中子,HmX分子,ag 1HmX所含质子数是 |
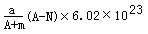
设氯原子的质量为ag,12C原子的质量为bg,用NA表示阿伏加德罗常数的值,则下列说法正确的是
| A.氯元素的相对原子质量为12/b | B.mg该氯原子的物质的量为m / NA mol |
| C.该氯原子的摩尔质量是a NA | D.ng该氯原子所含的电子数是17n/a |