根据下列五种元素的电离能数据(单位:kJ·mol-1),回答下面问题。
| 元素代号 |
I1 |
I2 |
I3 |
I4 |
| Q |
2 080 |
4 000 |
6 100 |
9 400 |
| R |
500 |
4 600 |
6 900 |
9 500 |
| S |
740 |
1 500 |
7 700 |
10 500 |
| T |
580 |
1 800 |
2 700 |
11 600 |
| U |
420 |
3 100 |
4 400 |
5 900 |
(1)在周期表中,最可能处于同一族的是( )。
A.Q和R
B.S和T
C.T和U
D.R和T
E.R和U
(2)电解它们的熔融氯化物,阴极电极反应式最可能正确的是( )。
A.Q2++2e-→Q
B.R2++2e-→R
C.S3++3e-→S
D.T3++3e-→T
E.U2++2e-→U
(3)它们的氯化物的化学式,最可能正确的是( )。
A.QCl2
B.RCl
C.SCl3
D.TCl
E.UCl4
(4)下列元素中,化学性质和物理性质最像Q元素的是( )。
A.硼(1s22s22p1)
B.铍(1s22s2)
C.锂1s22s1
D.氢(1s1)
E.氦(1s2)
某工业废水仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1 mol/L(此数值忽略水的电离及离子的水解)。
| 阳离子 |
K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
| 阴离子 |
Cl- CO32— NO3— SO42— I- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5 mL,滴加一滴氨水有沉淀生成,且离子种类增加。
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是___________________________________。
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是________________________。
(3)甲同学最终确定原溶液中所含阳离子有________,阴离子有________;并据此推测原溶液应该呈________性,原因是____________________________(请用离子方程式说明)。
(4)另取100 mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为____________________________。充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为________g。
柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3=FeCO3+Na2SO4
FeCO3+C6H8O7=FeC6H6O7+CO2+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| 金属离子 |
开始沉淀的pH |
沉淀完全的pH |
| Fe3+ |
1.1 |
3.2 |
| Al3+ |
3.0 |
5.0 |
| Fe2+ |
5.8 |
8.8 |
(1)制备FeCO3时,选用的加料方式是________(填字母),原因是_________________________________
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是_______________________________。
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌反应。
①铁粉的作用是_____________________。
②反应结束后,无需过滤,除去过量铁粉的方法是________________________________。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是__________________。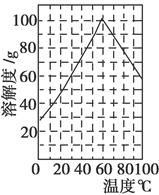
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合右图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应,________,得到FeSO4溶液,________,得到FeSO4·7H2O晶体。
中学常见的某反应的化学方程式为a+b―→c+d+H2O(未配平,反应条件已略去)。
请回答下列问题:
(1)若a是铁,b是稀硝酸(过量),且a可溶于c溶液中。则a与b反应的离子方程式为
___________________________。
(2)若c、d为气体,且都能使澄清石灰水变浑浊,则将此混合气体通入溴水中,橙色褪去,写出其褪色过程中发生反应的离子方程式:___________________________。
(3)若c是无色有刺激性气味的气体,其水溶液显弱碱性,在标准状况下用排空气法收集c气体,得平均摩尔质量为20 g·mol-1的混合气体进行喷泉实验。假设溶质不扩散,实验完成后烧瓶中所得溶液的物质的量浓度为________mol·L-1(小数点后保留2位有效数字)。
(4)若a是造成温室效应的主要气体,c、d均为钠盐,参加反应的a、b的物质的量之比为4:5。则上述反应的离子方程式为____________________________。
(1)以硫酸工业的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCl为原料可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸氢铵等物质.合成路线如下:
① 生产过程中,反应Ⅰ中需鼓入足量空气,试写出该反应的总方程式。
② 反应Ⅱ中需要向溶液中加入适量的对苯二酚等物质(已知对苯二酚具有很强的还原性),其作用可能是。
③ 反应Ⅲ中氧化剂与还原剂的物质的量之比为。
④ 能用于测定尾气中SO2含量的是 。
| A.滴有酚酞的NaOH溶液 | B.酸性KMnO4 |
| C.滴有淀粉的碘水 | D.BaCl2溶液. |
(2)已知铅蓄电池放电时发生如下反应:
负极:Pb-2e-+SO42-=PbSO4正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
如果用铅蓄电池做电源电解饱和食盐水制取Cl2,已知某铅蓄电池中硫酸溶液的体积为0.80L,电解前硫酸溶液浓度为4.50mol.L-1,当制得29.12 L Cl2时(指在标准状况下),求理论上电解后电池中硫酸溶液的浓度为(假设电解前后硫酸溶液的体积不变)________ mol.L-1。
钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大 量资金.请回答钢铁腐蚀与防护过程中的有关问题.
(1)钢铁的电化学腐蚀原理,在酸性环境中发生析氢腐蚀,在中性或碱性环境中发生吸氧腐蚀。
①分别写出图1中铁电极和石墨电极的电极反应式:
,。
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图1虚线框内所示
位置作出修改,并用箭头标出导线中电子流动方向。
③写出修改后石墨电极的电极反应式。
(2)工业上常用盐酸除去铁锈.现将一生锈的铁片放入盐酸中,溶液中可能发生的化学反应的化学方程式有 。
(3)在实际生产中,可在铁制品的表面镀铜防止铁被腐蚀.装置示意如图2:
①A电极对应的金属是(写元素名称),B电极的电极反应式是,
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为mol 。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因。