乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制备乙酸乙酯的化学方程式:CH3COOH+C2H5OH CH3COOC2H5+H2O,为证明浓硫酸在该反应中起到了催化剂和吸收剂的作用,某同学利用下图所示装置进行了以下四个实验,实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
CH3COOC2H5+H2O,为证明浓硫酸在该反应中起到了催化剂和吸收剂的作用,某同学利用下图所示装置进行了以下四个实验,实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验编号 |
试管Ⅰ中的试剂 |
试管Ⅱ中试剂 |
测得有机层的厚度/cm |
| A |
2 mL乙醇、2 mL乙酸、1 mL 18 mol·L-1浓硫酸 |
饱和碳酸钠溶液 |
5.0 |
| B |
3 mL乙醇、2 mL乙酸 |
0.1 |
|
| C |
3 mL乙醇、2 mL乙酸、6mL 3 mol·L-1硫酸 |
1.2 |
|
| D |
3 mL乙醇、2 mL乙酸、盐酸 |
1.2 |
(1)实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是________mL和________mol/L。
(2)分析实验________(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是_______________________________________________________________。
(3)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是____________________________________________(答出两条即可)。
实验室需要480 mL 0.4 mol·L-1的NaCl溶液,有如下操作步骤:
①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解.
②把①所得溶液小心转入一定容积的容量瓶中.
③继续向容量瓶中加蒸馏水至液面距刻度线1 cm~2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切.
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶.
⑤将容量瓶瓶塞塞紧,充分摇匀.
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)________.
(2)本实验用到的基本实验仪器除烧杯、玻璃棒外还需要的玻璃仪器是:___________.
(3)需要使用玻璃棒的操作有________(填序号).
(4)误差分析:(填“偏高”、“偏低”或“无影响”)
①称量NaCl时,把NaCl放在滤纸上称量__________.
②容量瓶没有完全干燥________.
③称量用的是生锈砝码________.
某研究性学习小组为了制取氨气和探究氨气的有关性质,进行了下列实验。
(1)根据图A氨气的制备装置制取氨气,试回答:收集氨气的方法是________________:装置中棉花的作用是_______________。
(2)甲、乙两组同学用干燥的圆底烧瓶各收集一瓶氨气,根据图B喷泉实验的装置进行实验,都观察到美丽的红色喷泉。
根据实验现象说明氨气具有的性质是____________________________________。
(3)甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图C所示。请通过分析确认:甲组同学所得氨水的物质的量浓度_______(填“大于”、“小于”或“等于”)乙组同学所得氨水的物质的量浓度。
某化学探究学习小组设计如下图装置制取硝酸(夹持和加热仪器均已略去)。实验中可供使用的药品有:Na2CO3、NaHCO3、NH4HCO3、Na2O2、NaOH溶液和水。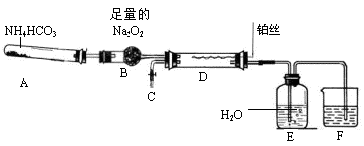
请回答下列问题:
(1)装置A中发生的化学反应方程式是。
(2)撤去装置D中的加热装置后,铂丝仍然保持红热,这是因为D中发生的化学反应是一个(填“放热”或“吸热”)反应。
(3)装置F中盛放的是溶液,其作用是。
(4)实验过程中,要使NH4HCO3充分转化为HNO3,还要在装置D中通入过量的氧气。甲同学提议在C处连接一个制取氧气的装置,乙同学认为可直接在A中再加入上述提供药品中的一种物质,这种药品的化学式是
如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响 因素,某同学做了如下探究实验:
因素,某同学做了如下探究实验:
| 序号 |
内容 |
实验现 象 象 |
| 1 |
常温下将铁丝放在干燥空气中一个 月 月 |
干燥的铁丝表面依然光亮 |
| 2 |
常温下将铁丝放在潮湿空气中一小时 |
铁丝表面依然光亮 |
| 3 |
常温下将铁丝放在潮湿的空气中一个月 |
铁丝表面已变得灰暗 |
| 4 |
将潮湿的铁丝放在高于常温的空气中一小时 |
铁丝表面已变得灰暗 |
| 5 |
将浸过氯化 钠溶液的铁丝放在高于常温的空气中一小时 钠溶液的铁丝放在高于常温的空气中一小时 |
铁丝表面灰暗程度比实验4严重 |
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是(填实验序号);在电化学腐蚀中,负极反应是;
(2)由该实验可知,可以影响铁锈蚀速率的因素是。
(3)为防止铁的锈蚀,工业上普遍采用的方法是(答两种方法)。
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3- )变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是 。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①3种溶液中,物质的量浓度最大的是 。
②分别用pH为0.1的NaOH溶液中和,其中消耗NaOH溶液最多的是 。
③反应开始时,反应速率 。
| A.HCl最快 | B.H2SO4最快 | C.CH3COOH最快 | D.一样快 |