如图是一个制取氯气并以氯气为原料进行特定反应的装置。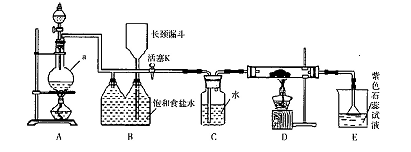
(l)A是氯气发生装置,写出其中的化学反应方程式 。
(2)a仪器的名称为 。
(3)实验开始时,先点燃A处的酒精灯,打开活塞K,让氯气充满整个装置,再点燃D处酒精灯,连接上E装置。D装置的硬质玻璃管内盛有炭粉,反应产物为CO2和HC1。写出D中反应的化学方程式 ,装置C的作用是 。
(4)在E处,若漏斗内气体带有黄绿色,则紫色石蕊试液的颜色变化为 。
(5)若将E处烧杯中溶液改为澄清石灰水,反应过程中现象为 (填序号)。
①有白色沉淀生成;②无白色沉淀生成;③先生成白色沉淀,而后白色沉淀消失。
(6)D处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2产生,则装置B
中的现象是 ;若发现装置B中该现象不明显,可能的原因是 ;查找原因时可用肥皂水或湿润的碘化钾淀粉试纸等,若用蘸有浓氨水的玻璃棒检查时观察到有白烟产生,写出该氧化还原反应的化学方程式 。
(1)用盐酸可以除去铜器表面的铜绿,该反应的化学方程式为:
____________________
(2)写出苯发生硝化反应的化学方程式:
___________________________________________________________________
布噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
请回答下列问题:
⑴A长期暴露在空气中会变质,其原因是。
⑵有A到B的反应通常在低温时进行。温度升高时,多硝基取代副产物会增多。下列二硝基取代物中,最可能生成的是。(填字母)
a. b.
b.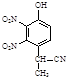 c.
c. d.
d.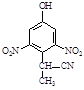
⑶在E的下列同分异构体中,含有手性碳原子的分子是。(填字母)
a.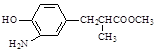 b.
b.
c. d.
d.
⑷F的结构简式。
⑸D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,则H的结构简式是。高聚物L由H通过肽键连接而成,L的结构简式是。
实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,解决下列问题:
⑴已知某反应的平衡表达式为:
它所对应的化学反应方程式为:
⑵利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g);ΔH=-90.8kJ·mol
CH3OH(g);ΔH=-90.8kJ·mol
②2CH3OH(g) CH3OCH3(g)+H2O(g);ΔH=-23.5kJ·mol
CH3OCH3(g)+H2O(g);ΔH=-23.5kJ·mol
③CO(g)+H2O(g) CO2(g)+H2(g);ΔH=-41.3kJ·mol
CO2(g)+H2(g);ΔH=-41.3kJ·mol
总反应:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的ΔH=__________
CH3OCH3(g)+CO2(g)的ΔH=__________
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g) H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
| 温度/℃ |
400 |
500 |
800 |
| 平衡常数K |
9.94 |
9 |
1 |
该反应的正反应方向是反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为:。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。
对反应:N2O4(g) 2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是。
2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是。
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
E.A、C两点的化学平衡常数:A>C
(5)CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。现在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。下列说法正确的是
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。现在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。下列说法正确的是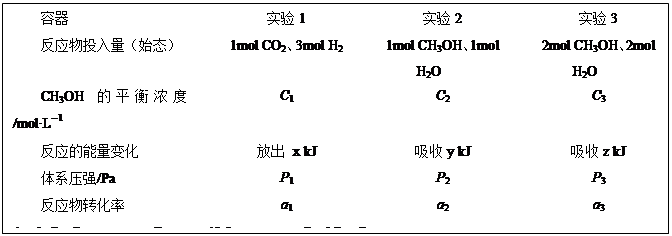
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3MgO、CaO等,生产工艺流程示意如下:
(1)将菱锌矿研磨成粉的目的是_____。
(2)完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+□____+□_____==□Fe(OH)3+□Cl-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为______。
| Mg(OH)2 |
Zn(OH)2 |
MgCO3 |
CaCO3 |
|
| 开始沉淀的pH[来源 |
10.4 |
6.4 |
— |
— |
| 沉淀完全的pH |
12.4 |
8.0 |
— |
— |
| 开始溶解的pH |
— |
10.5 |
— |
— |
| Ksp |
5.6×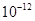 |
— |
6.8×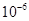 |
2.8×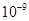 |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是______(选填序号)。
a.大理石粉b.石灰乳c.纯碱溶液d.烧碱溶液
(6)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________。
金刚石SiC具有优良的耐磨、耐腐蚀特性,应用广泛.
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物H为非极性分子,碳元素在周期表中的位置是,Q是,R的电子式为.
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为,除去粗产品中少量钠的试剂为.
(3)碳还原制SiC,其粗产品中杂质为Si和SiO2.先将20.0g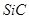 粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L,生成氢气的离子方程式为,硅酸钠的物质的量浓度为
粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L,生成氢气的离子方程式为,硅酸钠的物质的量浓度为
(4)下列叙述正确的有(填序号),
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应②水晶、干冰熔化时克服粒子间作用力的类型相同③Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2