下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是 ( )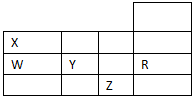
| A.常压下,五种元素的单质中,Z单质的沸点最高 |
| B.W的氢化物比X的氢化物的稳定性高 |
| C.Y、Z的阴离子电子层结构都与R原子的相同 |
| D.Y元素比W元素的非金属性强 |
下列化学键中,都属于极性共价键的是()
| A.共价化合物中的化学键 |
| B.离子化合物中的共价键 |
| C.同种元素原子间的共价键 |
| D.不同元素原子间的共价键 |
阴离子 含中子N个,X的质量数为A,则a gX的氢化物中含质子的物质的量是()
含中子N个,X的质量数为A,则a gX的氢化物中含质子的物质的量是()
A.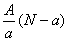 mol mol |
B. mol mol |
C. mol mol |
D.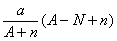 mol mol |
下列叙述正确的是()
| A.电子层数少的元素原子半径一定小于电子层数多的元素的原子半径 |
| B.核外电子层结构相同的单核微粒半径相同 |
| C.质子数相同的不同单核微粒,电子数越多,半径越大 |
| D.原子序数越大,原子半径越大 |
下列比较关系中,正确的是()
| A.元素金属性Na>Mg>Al | B.热稳定性H2S<H2Se<HCl |
| C.酸性H3PO3<H2SO4<HClO4 | D.原子半径Mg>Na>H |
下列对铯及其化合物的预测正确的是()
| A.铯的熔点很高 | B.在自然界中,铯能以游离态存在 |
| C.氯化铯易溶于水 | D.铯只有一种氧化物Cs2O |