天然海水中主要含有Na+、K+,Ca2+、Mg2+、Cl-、SO42—、Br-、CO32—、HCO3—等离子,火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示: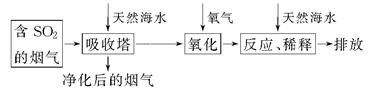
下列说法错误的是 ( )
| A.天然海水pH≈8的原因是海水中的CO32—、HCO3—水解 |
| B.“氧化”是利用氧气将H2SO3、HSO3—、SO32—等氧化生成SO42— |
| C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸 |
| D.“排放”出来的海水中SO42—的物质的量浓度与进入吸收塔的天然海水相同 |
溶液中存在有五种离子,其中各离子个数比Cl-∶SO42-∶Fe3+∶K+∶M=2∶3∶1∶3∶1,则M为( )
| A.CO32- | B.Mg2+ | C.Na+ | D.Ba2+ |
同温同压下两个容积相等的贮气瓶,一个装有C2H4,另一个装有C2H2和C2H6的混合气体,两瓶内的气体一定具有相同的 ()
| A.质量 | B.原子总数 | C.碳原子数 | D.密度 |
电影《闪闪的红星》中,为让被困的红军战士吃上食盐,潘冬子将浸透食盐水的棉袄裹在身上,带进山中……假如潘冬子在实验中,欲从食盐水中提取出食盐,最好采用的方法是( )
| A.过滤 | B.萃取 | C.蒸发 | D.蒸馏 |
下列物质中含原子个数最多是()
| A.0.4molO2 | B.5.6LCO2(标准状况) |
| C.4℃时5.4mLH2O | D.10gNe |
下列仪器中不能用于加热的是()
| A.试管 | B.烧杯 | C.量筒 | D.坩埚 |