亚硝酸钠(NaNO2)是一种常用的食品添加剂,具有防腐和增色作用。下列对亚硝酸钠性质的分析中,不合理的是( )
| A.亚硝酸钠中含有钠元素,焰色反应呈黄色 |
| B.已知亚硝酸为弱酸,则亚硝酸钠溶液呈碱性 |
| C.亚硝酸钠属于盐类物质,其水溶液能与金属钾反应生成金属钠 |
| D.亚硝酸钠中氮元素的化合价为+3,亚硝酸钠既具有氧化性又具有还原性 |
某同学按如图所示的装置进行实验,A、B为常见金属,它们的硫酸盐可溶于水。当K闭合后,在交换膜处SO42-从右向左移动。下列分析不正确的是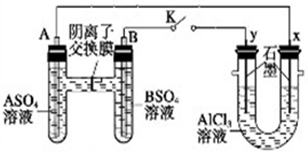
A、溶液中c(A2+)增大
B、B的电极反应:B2++2e-=B
C、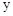 电极上有Cl2产生,发生氧化反应
电极上有Cl2产生,发生氧化反应
D、右边装置反应的离子方程式为:2Cl-+2H2O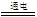 H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
下图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是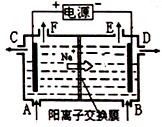
| A.从E口逸出气是H2 |
| B.从B中加入含少量NaOH的水溶液以增强导电性 |
| C.标准状况下每生成22.4L Cl2,可同时产生2molNaOH |
| D.若NaCl完全电解后加适量盐酸可以恢复到电解前的浓度 |
由环己烷、乙醇、乙醚组成的混合物,经测定碳的质量分数为72%,则氧的质量分数为
| A.19.6% | B.17.8% | C.16% | D.14.2% |
白磷与氧气可发生如下反应:P4+5O2===P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P  OckJ/mol、O
OckJ/mol、O  O dkJ/mol。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
O dkJ/mol。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
| A.(6a+5d-4c-12b)kJ/mol |
| B.(4c+12b-6a-5d)kJ/mol |
| C.(4c+12b-4a-5d)kJ/mol |
| D.(4a+5d-4c-12b)kJ/mol |
下列热化学方程式书写正确的是( 的绝对值均正确)
的绝对值均正确)
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g) kJ/mol(燃烧热) kJ/mol(燃烧热) |
B.NaOH(aq)+HCl (aq)===NaCl (aq) +H2O(l)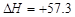 kJ/mol(中和热) kJ/mol(中和热) |
C.S(s)+O2(g)===SO2(g)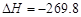 kJ/mol(反应热) kJ/mol(反应热) |
D.Fe+S===FeS kJ/mol(反应热) kJ/mol(反应热) |