有下列三个反应方程式:①Cl2+FeI2=FeCl2+I2 ②2Fe2++Br2=2Fe3++2Br- ③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O,下列说法正确的是 ( )。
| A.①②③中氧化产物分别是FeCl2、Fe3+、Cl2 |
| B.根据以上反应的化学方程式可以得到氧化性强弱关系为Cl2>Co2O3>Fe3+ |
| C.在反应③中生成1 mol Cl2时,有2 mol HCl被氧化 |
| D.根据反应①②一定可以推理得到Cl2+FeBr2=FeCl2+Br2 |
下列离子方程式书写正确的是( )
| A.硫酸镁溶液和氢氧化钡溶液反应:SO+Ba2+===BaSO4↓ |
| B.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O===AlO+4NH+2H2O |
C.苯酚钠溶液中通入过量的二氧化碳: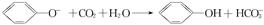 |
| D.氯化亚铁溶液中通入氯气:Fe2++Cl2===Fe3++2Cl- |
常温下,在溶液中可以发生反应:X+2Y3+===X2++2Y2+,则下列解释:①X被氧化;②X是氧化剂;③X具有还原性;④Y2+是氧化产物;⑤Y2+具有还原性;⑥Y3+的氧化性比X2+要强.其中正确的是( )
| A.②④⑥ | B.①③④ | C.②⑤ | D.①③⑤⑥ |
将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体,此液体不具有的性质是( )
| A.光束通过该液体时形成光亮的“通路” |
| B.插入石墨电极通直流电后,有一极附近液体颜色加深 |
| C.向该液体中加入硝酸银溶液,无沉淀产生 |
| D.将该液体加热、蒸干、灼烧后,有氧化物生成 |
“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸⑥静置后会析出黑色沉淀
| A.①④⑤ | B.②③④ | C.②③⑤ | D.①③④⑥ |
一定温度下,可逆反应A(s)+2B(g) 2C(g)+D(g);△H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。
2C(g)+D(g);△H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。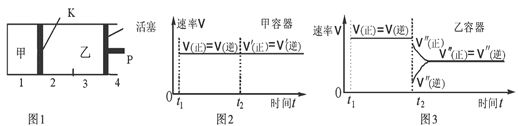
下列说法正确的是
| A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持活塞位置不变,改变温度,达到新的平衡后,甲、乙中B的体积分数均增大 |