A、B、C、D、E是原子序数依次增大的五种短周期元素,且B、C相邻,A元素可以与B、C、E元素分别形成化合物甲、乙、丙,甲、乙均为10电子分子,丙为18电子分子。D元素的原子最外层电子数与核外电子层数相等。已知:甲+E2=丙+B2,甲+丙=丁,下列说法正确的是( )。
A.离子半径:D>C>B
B.BE3分子中,中心原子杂化类型是sp2杂化
C.甲、乙、丙、丁四种物质的晶体类型均为分子晶体
D.A与C两种元素共同形成的10电子粒子有3种
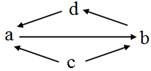
下表所列各组物质中,物质之间通过一步反应无法实现如图所示转化的是
| 物质转化关系 |
a |
b |
c |
d |
|
| A |
 |
FeCl2 |
FeCl3 |
Fe[ |
CuCl2 |
| B |
SO2 |
SO3 |
S |
H2SO4 |
|
| C |
CH2ClCH2Cl |
CH≡CH |
CH2OHCH2OH |
CH2=CH2 |
|
| D |
Al2O3 |
NaAlO2 |
Al |
Al(OH)3 |
下列有关实验操作或判断正确的有
①用10 mL量筒准确量取稀硫酸溶液8.0 mL;
②用干燥的pH试纸测定氯水的pH;
③能说明亚硝酸是弱电解质的是:用HNO2溶液作导电试验,灯泡很暗
④使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大;
⑤将饱和FeCl3溶液滴入蒸馏水中即得Fe(OH)3胶体;
⑥圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上
⑦除去铁粉中混有的少量铝粉.可加人过量的氢氧化钠溶液,完全反应后过滤
⑧为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
⑨用食醋除去水壶中的水垢
| A.3个 | B.4 个 | C.5个 | D.6个 |
工业上常将铬镀在其他金属表面,同铁.镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,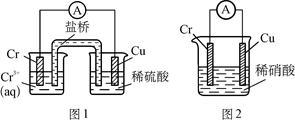
铬电极上产生大量有色气体,则下列叙述正确的是( )
| A.图1为原电池装置,Cu电极上产生的是O2 |
| B.图2装置中Cu电极上发生的电极反应式为:Cu-2e-===Cu2+ |
| C.由实验现象可知:金属活动性Cu>Cr |
| D.两个装置中,电子均由Cr电极流向Cu电极 |
实验表明,相同温度下,液态纯硫酸的导电性强于纯水。已知液态电解质都能像水那样自身电离而建立电离平衡(如H2O+H2O H3O++OH-),且在一定温度下都有各自的离子积常数。25 ℃时,纯硫酸的离子积常数K和水的离子积常数Kw关系为( )
H3O++OH-),且在一定温度下都有各自的离子积常数。25 ℃时,纯硫酸的离子积常数K和水的离子积常数Kw关系为( )
| A.K>Kw | B.K=Kw | C.K<Kw | D.无法比较 |
设nA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A.7 g CnH2n中含氢原子数为nA |
| B.4.6 g NO2.N2O4混合气体中含有中子数为2.3nA |
C.在反应5NH4NO3 2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为15 nA 2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为15 nA |
| D.电解精炼铜时每转移nA个电子,阳极溶解32 g铜 |