下列关于各溶液的描述中正确的是 ( )。
| A.pH相等的①NH4Cl,②(NH4)2SO4,③NH4HSO4的溶液中,c(NH4+)大小:①=②=③ |
| B.常温下,在10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20 mL |
| C.向1.00 L 0.3 mol·L-1的NaOH溶液中缓慢通入CO2气体至溶液增重8.8 g,所得溶液中:3c(Na+)=2[c(HCO3—)+c(CO32—)+c(H2CO3)] |
| D.浓度均为0.1 mol·L-1的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-) |
已知:将Cl2通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且 的值仅与温度高低有关。当n(NaOH)="6a" mol时,下列有关说法不正确的是
的值仅与温度高低有关。当n(NaOH)="6a" mol时,下列有关说法不正确的是
| A.改变温度,反应中转移电子的物质的量n的范围:3a mol≤n≤5a mol |
| B.改变温度,产物中NaCl的最小理论产量为4a mol |
| C.参加反应的氯气的物质的量3a mol |
D.某温度下,若反应后 =6,则溶液中 =6,则溶液中 =6 =6 |
某同学组装了如图所示的电化学装置,则下列说法正确的是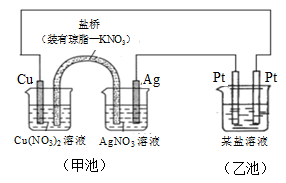
| A.图中甲池为原电池装置,Cu电极发生还原反应 |
| B.实验过程中,甲池左侧烧杯中NO3-的浓度不变 |
| C.若甲池中Ag电极质量增加5.4 g时,乙池某电极析出1.6 g金属,则乙中的某盐溶液可能是AgNO3溶液 |
| D.若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量会减小 |
在体积均为1.0 L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s)  2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
| A.化学平衡常数K:K(状态I)<K(状态II)<K(状态III) |
| B.CO2的平衡转化率α:α(状态I)<α(状态Ⅱ)=α(状态III) |
| C.体系中c(CO):c (CO,状态Ⅱ)<2c (CO,状态Ⅲ) |
| D.逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ) |
以0.10 mol/L的氢氧化钠溶液滴定某一元酸HA的滴定曲线如图所示。下列表述正确的是
| A.此实验可以选用甲基橙作指示剂 |
| B.该酸HA的浓度约为1×10-4 mol/L |
| C.当NaOH体积为9 mL时,恰好完全中和反应 |
| D.达到滴定终点时,溶液中c(Na+)>c (A-) |
在酸性Fe(NO3)3溶液中逐渐通入H2S气体,不可能发生的离子反应是
| A.3H2S+2NO3-+2H+ =2NO↑+3S↓+ 4H2O |
| B.3Fe3++ 3NO3-+6H2S =3NO↑+ 6S↓+3Fe2++6H2O |
| C.Fe3++3NO3-+5H2S+2H+=3NO↑+5S↓+Fe2++6H2O |
| D.Fe3++9NO3-+14H2S+ 8H+=9NO↑+14S↓+Fe2++18H2O |