(创新预测题)已知25 ℃时弱电解质的电离平衡常数:
Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13。
(1)将20 mL 0.10 mol·L-1 CH3COOH溶液和20 mL 0.10 mol·L-1的HSCN溶液分别与0.10 mol·L-1的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与
时间t的关系如图所示。
反应开始时,两种溶液产生CO2的速率明显不同的原因是________;反应结束后所得溶液中c(SCN-)______c(CH3COO-)(填“>”、“=”或<)。
(2)2.0×10-3 mol·L-1的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液pH的关系如图所示。则25 ℃时,HF电离平衡常数为Ka(HF)=________(列式求值)。
(3)难溶物质CaF2溶度积常数为Ksp=1.5×10-10,将4.0×10-3 mol·L-1 HF溶液与4.0×10-4 mol·L-1的CaCl2溶液等体积混合,调节溶液pH=4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成?________(填“有”或“没有”),简述理由:_____________________________________。
工业生产粗硅的反应有:
SiO2+2C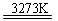 Si(粗)+2CO↑;SiO2+3C
Si(粗)+2CO↑;SiO2+3C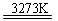 SiC+2CO↑。
SiC+2CO↑。
(1)若产品中粗硅与碳化硅的物质的量之比为1∶1,则参加反应的C 和SiO2的质量比为______________。
(2)粗硅进一步制备纯硅的原理如下:
Si(粗)+2Cl2(g)  SiCl4(l); SiCl4+2H2
SiCl4(l); SiCl4+2H2 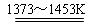 Si(纯)+4HCl。
Si(纯)+4HCl。
若上述反应中Si(粗 )和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产25.2吨纯硅需纯度为75%石英砂_______________吨。
)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产25.2吨纯硅需纯度为75%石英砂_______________吨。
(3)工业上还可以通过如下图所示的流程制取纯硅:
若反应①为:Si(粗)+3HCl(g)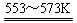 SiHCl3(l)+H2(g);
SiHCl3(l)+H2(g);
则反应②的化学方程式为___________________________________ 。
假设每一轮次生产过程中,硅元素没有损失,反应①中HCl的利用率为α1,反应②中H2的利用率为α2,,若制备1mol纯硅,在第二轮次的生产中,现补充投入HCl和H2的物质的量之比是5∶1。则α1与α2的代数关系式为____________________________。
已知①R—X+NaCN R—CN+NaX;
②R—CN+H2O R—COOH
R—COOH
某高效、低毒的农药K的合成路线如下:(部分无机物已省略)
(1)C→D的反应类型_________________ ;
(2)A的结构简式____________________ ;
(3)写出G→ H反应的化学方程式_____________________________________ ;
(4)M的同分异构体有多种,写出具有下列性质的同分异构体的结构简式:_________________;
①能与FeCl3溶液发生显色反应
②能发生银镜反应
③核磁共振氢谱有四个峰
(5)写出由 制备高分子化合物
制备高分子化合物 的合成路线流程图(无机试剂任选)。
的合成路线流程图(无机试剂任选)。
合成路线流程图示例如下:
高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:
3NaClO + 2Fe(NO3)3 + 10NaOH=2Na2FeO4↓+ 3NaCl + 6NaNO3 + 5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
主要的生产流程如下:
(1)写出反应①的离子方程式_____________________________。
(2)流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4) _________ Ksp(Na2FeO4)(填“>”或“<”或“=”)。
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响。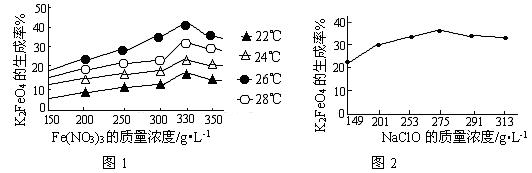
①工业生产中最佳温度为_______℃,此时Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为_______。
②若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:
____________________________________________________。
若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:____________________________________。
(4)K2FeO4 在水溶液中易水解:4FeO42—+10H2O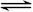 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______溶液(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______溶液(填序号)。
| A.H2O | B.CH3COONa、异丙醇 | C.NH4Cl、异丙醇 | D.Fe(NO3)3、异丙醇 |
二甲基亚砜有消炎止痛、镇静等作用。甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3—S—CH3),甲硫醚再与NO2反应制取二甲基亚砜 (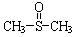 ),有关反应如下:
),有关反应如下:
反应① 2CH3OH(l)+H2S(g)=(CH3)2S(l) +2H2O(l)△H=―akJ·mol-1
反应② (CH3)2S(l)+NO2(g)=(CH3)2SO(l)+NO(g)△H=-bkJ··mol-1
反应③ 2NO(g)+O2(g)=2NO2(g)△H=-ckJ·mol-1
(1)写出用甲硫醚直接和氧气反应制取二甲基亚砜的热化学反应方程式
___________________________________________________, (2)能说明反应2CH3OH(l)+H2S(g) (CH3)2S(l) +2H2O(l)达平衡状态的是____________ 。
(2)能说明反应2CH3OH(l)+H2S(g) (CH3)2S(l) +2H2O(l)达平衡状态的是____________ 。
| A.v(CH3OH) =" 2v(H2S)" |
| B.恒容容器中,体系的压强不再改变 |
| C.恒容容器中,体系中气体的密度不再改变 |
D.恒容容器中,气体的摩尔质量不 再改变 再改变 |
(3)反应③在一定条件下可达到平衡,则此条件下该反应平衡常数表达式K= ____________________。
(4)N2O5是一种新型绿色硝化剂,其制备方法有以下两种。
方法一:4NO2(g)+O2(g) =2N2O5(g)  ;△H=-56.76 KJ·mol-1
;△H=-56.76 KJ·mol-1
常温下,该反应能逆向自发进行,则逆向反应的△S __________ 0(填“>、<”或“=”)
方法二:用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5。工作原理如下图: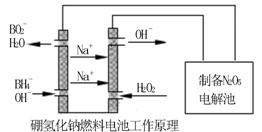
硼氢化钠燃料电池的正极反应式________________________。
化合物G是冶炼某常见金属的原料,工业上提取G的流程如下图所示(已知晶体E的焰色反应呈黄色):
(1)溶液A为_____________溶液(用化学式表示,下同),赤泥浆C的主要成分有_____________ ,
(2)操作Ⅰ为_____________;操作Ⅱ为_____________ ,
(3)写出由B生产F的离子方程式为_________________________________
(4)苛化试剂与E溶液反应生成溶液A,则苛化试剂是_____________ ,该工艺的优点是_____________(答一条,合理即可)。