电解是最强有力的氧化还原手段,在化工生产中有着重要的应用。请回答下列问题:
(1)以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为________,阴极反应式为________。
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是______________________________________(填序号)。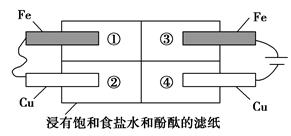
a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O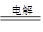 CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH
实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。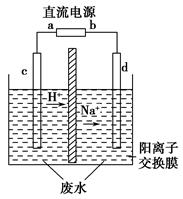
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入________(填化学式),电极反应式为________。电解过程中,阴极区Na2SO4的物质的量________(填“增大”、“减小”或“不变”)。
②在实际工艺处理中,阴极区乙醛的去除率可达60%。若在两极区分别注入1 m3乙醛含量为3 000 mg/L的废水,可得到乙醇________kg(计算结果保留小数点后1位)。

(1)已知某温度下,反应2SO2+O2 2SO3,的平衡常数K=19,在该温度下的体积
2SO3,的平衡常数K=19,在该温度下的体积 固定的密闭容器中充
固定的密闭容器中充 入C(SO2)=1mol·L-1,C(O2)="1" mol·L-1,当反应在该温度下SO2转化率
入C(SO2)=1mol·L-1,C(O2)="1" mol·L-1,当反应在该温度下SO2转化率 为80%时,该反应
为80%时,该反应
(填“是”或“否”)达到化学平衡状态,若未达到,向 (填“正反应”或“逆反应”) 方向进行。
(填“正反应”或“逆反应”) 方向进行。
(2)对于可逆反应:aA(g) +bB(g)  cC(g)+dD(g)△H = a kJ·mol
cC(g)+dD(g)△H = a kJ·mol -1;
-1;
若增大压强平衡向正反应方向移动,则a+bc+d(填“>”或“<”);若升高温度,平衡向正反应方向移动,则a_______0(填“>”或“<”)
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g)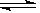 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)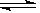 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)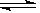 SO3(g)+NO(g)的ΔH=kJ·mol-1。
SO3(g)+NO(g)的ΔH=kJ·mol-1。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=。(保留2位小数)
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)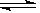 CH3OH(g)。
CH3OH(g)。
CO在不同温度下的平衡转化率与压强的关系如图所示。
该反应ΔH0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是。
25℃时,①醋酸②次氯酸③氢氟酸的电离常数分别是1.8×10-5、3.0×10-8、3.5×10-4。请推测:
(1)它们的酸性由强到弱的顺序为______________________(填序号,下同),
(2)相同浓度的溶液中,氢离子浓度最大的是___________;
(3)氢离子浓度相同的溶液中,酸的浓度最大的是。
把煤作为燃料可以通过下列两种途径:
途径I:C(s)+O2(g) CO2(g) ΔH=E1 ①
CO2(g) ΔH=E1 ①
途径II:先制水煤气:C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
再燃烧水煤气:H2(g)+1/2O2(g) H2O(g) ΔH=E3③
H2O(g) ΔH=E3③
CO(g)+1/2O2(g) CO2(g) ΔH=E4④ ,试回答下列问题:
CO2(g) ΔH=E4④ ,试回答下列问题:
(1)判断两种途径放热:途径I放出的热量 _____(填“大于”、“等于”、“小于”)途径II放出的热量。
_____(填“大于”、“等于”、“小于”)途径II放出的热量。
(2)E1、E2、E3、E4的数学关系式 是_____________________________________。
是_____________________________________。
(3)由于制取水煤气反应里,反应物所具有的总能量_______(填“大于”、“等于”、“小于”)生成物所具有的总能量,正反应又是熵增加的反应,为了让该反应自发进行,要使反应条件为_______。
苯乙烯是一种重要的化工合成原料。现由苯乙烯合成聚三溴代苯乙烯和另外一种高聚物M的工艺如下:
已知:苯环上的取代反应有如下定位规律:当苯环上已经有了一个取代基时,新引进的取代基因受原取代基的影响而取代其邻、对位或间位的氢原子。使新取代基进入它的邻、对位的取 代基有—R(烷基)、—NH2等;使新取代基进入间位的取代基有—COOH、—NO2等;
代基有—R(烷基)、—NH2等;使新取代基进入间位的取代基有—COOH、—NO2等;
(1)D是高分子化合物,写出D的结构简式______________。
(2)①②③④⑤反应中属于取代反应的是________;
反应⑧的类型为________ 。
(3)设计反应①、③的目的是_______
(4)写出下列反应的化学方程式
反应③:________
反应⑦:________
(5)G有多种同分异构体,写出任意一个符合下列条件的同分异构体的结构简式________ 。
①能发生银镜反应;②能与FeCl3溶液发生显色反应;
③核磁共振谱氢图中出现6组吸收峰。