纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:___________________________。
(2)写出“联合制碱法”有关反应的化学方程式:_______________________
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?_______________________。
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应列出计算原子利用率的表达式:原子利用率(%)=_________________。
(1)按官能团的不同可以对有机物进行分类,请指出下列有机物的种类,填在横线上。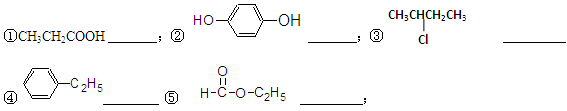
(2)化合物A和B的分子式都是C2H4Br2, A的核磁共振氢谱图如图所示,则A的结构简式为:,请预测B的核磁共振氢谱上有个峰(信号)。
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。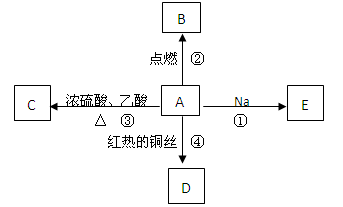
(1)写出A的化学式。
(2)下列反应的化学方程式
反应①;
反应③;
反应④。
(3)比较反应①与钠和水反应的现象有什么相同和不同。
相同点: ;
不同点:
(8分)在利用CaCO3与盐酸反应制取二氧化碳的反应中,反应中生成二氧化碳的体积与反应时间的关系如图所示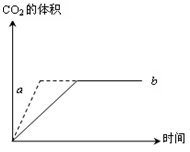
两个实验所用的盐酸浓度相同,其中一个实验用是石灰石块,,另一实验用是石灰石粉末,则从图中可以看出:
①使用石灰石块的是 (填a或b,下同),反应速率较快的曲线是,由b图变为a的原因是  ②如果实验过程中所用的盐酸是过量的,则所取块状石灰石与粉末状石灰石的质量是否相等?(填“相等”或“不相等”)。
②如果实验过程中所用的盐酸是过量的,则所取块状石灰石与粉末状石灰石的质量是否相等?(填“相等”或“不相等”)。
将20g Ba(OH)2·8H2O晶体与10 g NH4Cl晶体一起放入小烧杯中,将烧杯放在滴有3~4滴水的玻璃片上,用玻璃棒迅速搅拌。
(1)写出有关反应的化学方程式。
(2)实验中观察到的现象有、和反应混合物成糊状
(3)通过现象,说明该反应为(填“吸热”或“放热”)反应,这是由于反应物的总能量(填“小于”或“大于”)生成物的总能量
对于反应2S02+02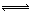 2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
| 编号 |
改变的条件 |
生成SO3的速率 |
| ① |
升高温度 |
|
| ② |
降低温度 |
|
| ③ |
增大氧气的浓度 |
|
| ④ |
使用催化剂 |
|
| ⑤ |
压缩体积 |
|
| ⑥ |
恒容下充人Ne |