工厂的工业废水,不可直接往江河湖海中排放,否则会造成严重公害。某河道两旁有甲、乙两厂,它们排出的工业废水各含有K+、Fe3+、Ba2+、Ag+、Cl-、SO42-、NO3-、OH-中的四种。又知甲厂污水pH>7。
(1)甲厂污水中含有的四种离子可能是:_______________________________。
(2)乙厂污水中含有的四种离子可能是:______________________________。
(3)对乙厂废水进行处理,方法之一,可往废水中加入一定量的________(选填
“活性碳”“硫酸亚铁”或“铁粉”),可以回收其中的金属__________(填
元素符号)。
(4)消除污染的另一种重要措施是将甲、乙两厂的废水按比例混合,可使废水中的________(填离子符号)转化为沉淀,从而大大降低污染程度。过滤后所得废水主要含________,可用于浇灌农田。
Ⅰ.硼元素B在化学中有很重要的地位。硼的化合物在农业、医药、玻璃工业等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布简式 。从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序为 。
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料。同数原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是 。
(3)在BF3分子中中心原子的杂化轨道类型是 ,SiF4微粒的空间构型是 。又知若有d轨道参与杂化,能大大提高中心原子成键能力,试解释为什么BF3、SiF4水解的产物中,除了相应的酸外,前者生成BF4-,后者却是生成SiF62-: 。
Ⅱ.图所示为血红蛋白和肌红蛋白的活性部分---血红素的结构: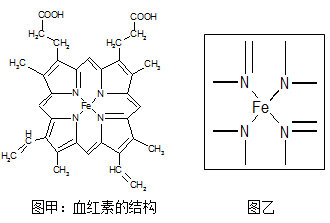
回答下列问题:
(1)根据元素电负性请判断H2N-CHO中碳和氮的化合价分别为 和 。
(2)血红素中两种氮原子的杂化方式分别为 , ;在图乙的方框内用“→”标出亚铁离子的配位键。
世界环保联盟建议全面禁止使用氯气对饮用水进行消毒,而建议采用高效“绿色‘消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体、易溶于水,不稳定,呈黄绿色。在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备二氧化氯的流程如图:
(1)二氧化氯中所有原子 (填“是”“不是”)都满足8电子结构。如图所示,用电解法制得的产物中,杂质气体B能是石蕊试液显蓝色,除去杂质气体可选用 (填序号)。
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品。下列说法正确的是 (填序号)。
A.二氧化氯克广泛用于工业和饮用水处理
B.二氧化氯的消毒效率比氯气的消毒效率高
C.稳定性二氧化氯的出现大大增加了二氧化硫的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用铝酸钠氧化浓盐酸制备二氧化氯。化学反应方程式为 。缺点主要是产率低,产品难以分离。还可能污染环境。
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备二氧化氯,化学方程式为 。此法相比欧洲方法的优点是 。
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的操作(H2C2O4)溶液还原铝酸钠,化学反应方程式为 。此法提高了生产及储存、运输的安全性,原因是。
草酸(乙二酸)可做还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工艺流程如图。
回答下列问题:
(1)CO和氢氧化钠在一定条件下合成甲酸钠的化学反应方程式为 。
(2)该制备工艺中有两次过滤操作,过滤操作②的滤液是 ,滤渣是 。
(3)工艺过程中③和④的目的是 。
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸,该方案的缺点是产品不纯,其中含有的杂质主要是 。
(5)结晶水合草酸成品的纯度用高锰酸钾法测定,称量草酸成品0.250g溶于水,用0.05000mol/L的酸性高锰酸钾溶液滴定,至浅红色不消退,消耗高锰酸钾溶液15.00mL,反应的离子方程式为 ;列式计算该成品的纯度 。
氮及其化合物在生活、生产和科技等方面有重要的应用。砷位于周期表中的第四周期,与氮元素属同一主族元素,其广泛分布与自然界。试回答下列问题:
(1)砷的气态氢化物的电子式为 。
(2)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮做催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2:1,写出该反应的化学方程式: 。
(3)砷的常见酸性氧化物有As2O3和As2O5,请根据图相关信息写出分解为的热化学方程式: 。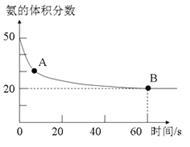
(4)直接供氨式碱性燃料电池的电池反应式为4NH2+3O2=2N2+6H2O,电解 质溶液一般使用氢氧化钾溶液,则负极电极反应式为 。
(5)氨气和二氧化碳在120℃,催化剂作用下反应生成尿素:CO2(g)+2NH3(g) 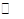 (NH2)2CO(s)+H2O(g),在密闭反应容器中,混合气体中氨气的含量变化关系如图所示,则氨气的平衡转化率是 。
(NH2)2CO(s)+H2O(g),在密闭反应容器中,混合气体中氨气的含量变化关系如图所示,则氨气的平衡转化率是 。
(6)将一定量的NH2COONH4(s)置于恒温密闭容器中,NH2COONH4(s) 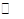 2NH3(g)+CO2(g),其分解达到平衡状态时,该反应的化学平衡常数的表达式为 。
2NH3(g)+CO2(g),其分解达到平衡状态时,该反应的化学平衡常数的表达式为 。
(7)在容积恒定的密闭容器中进行反应2NO(g)+O2(g) 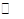 2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是 (填序号)
2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是 (填序号)
a.在t1-t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t3-t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t5时,容器内NO2的体积分数是整个过程中的最大值
已知Cr(OH) 3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。因此,必须对含铬的废水进行处理,可采用以下两种方法。
还原法在酸性介质中用FeSO4等将+6价铬还原成+3价铬。具体流程如下: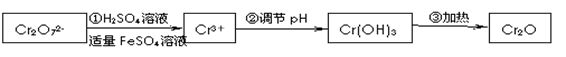
有关离子完全沉淀的pH如下表:
| 有关离子 |
Fe2+ |
Fe3+ |
Cr3+ |
| 完全沉淀为对应氢氧化物的pH |
9.0 |
3.2 |
5.6 |
(1)写出Cr2O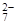 与FeSO4溶液在酸性条件下反应的离子方程式__________________。
与FeSO4溶液在酸性条件下反应的离子方程式__________________。
(2)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。
则在操作②中可用于调节溶液pH的试剂最好为:_____________(填序号);
A.Na2O2 B.Ca(OH)2 C.Ba(OH)2 D.NaOH
此时调节溶液的pH范围在____________(填序号)最佳。
A.12~14 B.10~11 C.6~8 D.3~4
(3)将等体积的4.0×10-3mol·L-1的AgNO3和4.0×10-3mol·L-1的K2CrO4溶液混合能析出Ag2CrO4沉淀(Ksp(Ag2CrO4)=9.0×10-12),请写出表示Ag2CrO4溶解平衡的方程式,并简要写出能生成Ag2CrO4沉淀原因的计算过程。