海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下: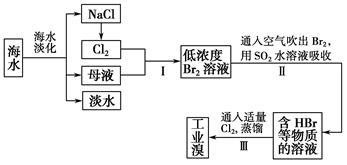
(1)请列举海水淡化的两种方法:________、________。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、________、________或H2、________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为___________ _____________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________________________,
由此反应可知,除环境保护外,在工业生产中应解决的主要问题是______________________________。
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图: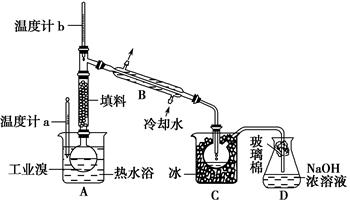
请你参与分析讨论:
①图中仪器B的名称:____________________________________________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是_________ ________________________________________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:_________________________________。
④C中液体产物颜色为________,为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是_____________________。
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是
A.CH3OH(l)+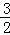 O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol |
| B.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣1452kJ/mol |
| C.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣725.8kJ/mol |
| D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1452kJ/mol |
用0.01mol·L-1 NaOH 溶液完全中和pH=3的下列溶液各100mL。需NaOH溶液体积最大的是
| A.盐酸 | B.硫酸 | C.高氯酸 | D.醋酸 |
下列对化学反应的认识,错误的是
| A.会引起化学键的变化 | B.会产生新物质 |
| C.必然引起物质状态的变化 | D.必然伴随着能量的变化 |
将V1 mL l.0mol/L盐酸和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V2+V2=50ml).下列叙述正确的是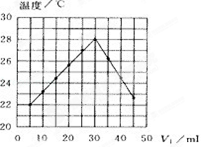
| A.做该实验时环境温度为22℃ |
| B.该实验表明化学能可能转化为热能 |
| C.NaOH溶液的浓度约为1.0 mol/L |
| D.该实验表明有水生成的反应都是放热反应 |
下列说法不正确的是
| A.在化学反应进行的过程中放出或吸收的热量称为反应热 |
| B.在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热 |
| C.对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量 |
| D.在101Kpa时,1mol物质完全燃烧生成稳定氧化物时,所放出的热量叫做该物质的燃烧热 |