在硫酸铝、硫酸钾和明矾[KAl(SO4)2·12H2O]混合溶液中,SO42—浓度为0.4mol/L,当加入等体积0.4mol/L KOH溶液时,生成的沉淀恰好完全溶解。则反应后溶液中K+的浓度约为( )
| A.0.225mol/L | B.0.25mol/L | C.0.45mol/L | D.0.9mol/L |
用下图表示的一些物质或概念之间的从属或包含关系中,错误的是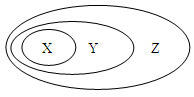
| X |
Y |
Z |
|
| 例 |
氧化物 |
化合物 |
纯净物 |
| A |
碘酒 |
分散系 |
混合物 |
| B |
液氨 |
电解质 |
化合物 |
| C |
胆矾 |
正盐 |
纯净物 |
| D |
NaHSO4 |
酸式盐 |
电解质 |
在同温同压下,A容器中的氧气(O2)和B容器中的氨气(NH3)所含的原子个数相同,则A、B两容器中气体的体积之比是
A.1:2 B.2:3 C.2:1 D.3:2
判断下列有关化学基本概念的依据正确的是
| A.溶液与胶体:不同的本质原因是能否发生丁达尔效应 |
| B.纯净物与混合物:是否仅含有一种元素 |
| C.氧化还原反应:元素化合价是否变化 |
| D.电解质与非电解质:物质本身的导电性 |
下列属于电解质并能导电的物质是
| A.液态氯化氢 | B.KNO3溶液 | C.氯化钠晶体 | D.熔融的Na2O |
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是
| A.甲的分子数比乙的分子数多 |
| B.甲的物质的量比乙的物质的量少 |
| C.甲的摩尔质量比乙的摩尔质量小 |
| D.甲的相对分子质量比乙的相对分子质量小 |