贝诺酯是一种治疗类风湿险关节炎药物,其结构简式如图所示,下列关于贝诺酯的描述正确的是( )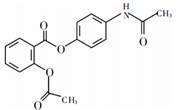
| A.贝诺酯使溴水和酸性高锰酸钾溶液褪色的原理相同 |
| B.贝诺酯中含有3种含氧官能团 |
| C.1 mol贝诺酯最多可以消耗9 mol H2 |
| D.1 mol贝诺酯最多可以消耗5 mol NaOH |
既能透过半透膜,又能透过滤纸的是()
| A.NaCl溶液 | B.淀粉溶液 | C.酒精溶液 | D.Fe(OH)3胶体 |
将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是 ( )
| A.稀硫酸 | B.氯水 | C.硝酸锌 | D.双氧水 |
下列块状金属在常温时能全部溶于足量浓HNO3的是 ()
| A.Ag | B.Cu | C.A1 | D.Fe |
下列有关使用托盘天平的叙述,不正确的是().
| A.称量前先调节托盘天平的零点 |
| B.称量时左盘放被称量物,右盘放砝码 |
| C.潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量 |
| D.用托盘天平可以准确称量至0.01克 |
关于化学键的下列叙述中,正确的是 ( )
| A.离子化合物可能含共价键 | B.共价化合物可能含离子键 |
| C.离子化合物中只含离子键 | D.NH4Cl晶体中只有共价键 |