下列反应的离子方程式中正确的是
| A.过氧化钠与水反应:O22- + 2H2O =2OH- + H2↑ |
| B.用纯碱溶液溶解苯酚:CO32-+2C6H5OH = 2C6H5O- + CO2↑+H2O |
C.用石墨作电极电解AlCl3溶液:2Cl- + 2H2O  Cl2↑ + H2↑ + 2OH- Cl2↑ + H2↑ + 2OH- |
| D.将0.2 mol/L的NH4Al(SO4)2溶液与0.3 mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-= 2Al(OH)3↓+3BaSO4↓ |
强酸与强碱的稀溶液发生中和反应的热效应为:
H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ·mol-1。分别向1L 0.5mol/L的NaOH溶液中加入①浓硫酸;②稀硫酸;③稀盐酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是( )
| A.△H1>△H2>△H3 | B.△H1<△H2<△H3 |
| C.△H1<△H2=△H3 | D.△H1=△H2<△H3 |
某同学为了使反应2HCl + 2Ag 2AgCl + H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是()
2AgCl + H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是()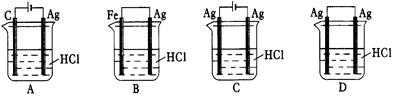
以惰性电极电解下列物质的水溶液(电解质均过量),电解后溶液pH升高的是()
①盐酸②硫酸③氢氧化钾④氯化钾⑤硝酸银⑥硫酸钠
| A.①②③ | B.④⑤⑥ | C.①③④ | D.②⑤⑥ |
25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量。下列表示该反应的热化学方程式中正确的是()
| A.CH3OH(l)+3/2O2(g) = CO2(g) +2H2O(l) △H=-725.8 kJ·mol-1 |
| B.2 CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(l) △H="+1451.6" kJ·mol-1 |
| C.2 CH3OH+O2 = 2CO2+4H2O△H=-22.68 kJ·mol-1 |
| D.CH3OH(l)+3/2O2(g) = CO2(g)+2H2O(g)△H=-725.8 kJ·mol-1 |
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为()
A、 A﹥B﹥E﹥D B、 A﹥B﹥D﹥E
C、 D﹥E﹥A﹥B D、 D﹥A﹥B﹥E