水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)“生命吸管”(如图)是一种可以随身携带的小型水净化器,里面装有网丝,注入了活性炭和碘的树脂等。其中活性炭起到________________和过滤的作用。
(2)水常用来配制各种溶液,硝酸钾溶液中的溶质为_________________。
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为__________g。
(4)根据下表回答问题。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
| 溶解度/g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
| NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.6 |
77.3 |
①60 ℃时,向两个分别盛有50 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为饱和溶液的是____________溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法正确的是___________(填字母序号)。
A.溶质的质量不变
B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变
D.可升高温度或增加溶剂
根据物质的什么具体性质鉴别下列各组物质。
(1)厨房里的糖和食盐:;(2)白酒和食醋:;
(3)面粉和洗衣粉:;(4)铜丝和铁丝:。
某同学用实验室常用仪器组装成如下实验装置,请回答下列问题: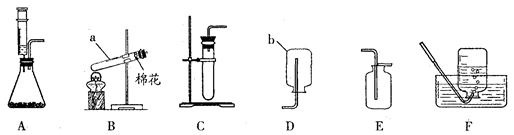
(1)写出标有字母的仪器名称:
,
.
(2)若用装置
制备氧气,仪器
中装有高锰酸钾,还需作的一点改动是.
(3)若用装置
或
及相关药品制备氧气,则反应的化学方程式是;与装置
相比,装置
的优点是(只要求写出一点);收集氧气应选用的装置是(填字母代号)或.
(4)用装置
或
及相关药品还可制备(填一种气体的化学式).
在上海世博园江苏馆的"春华秋实"展区,用我市东海水晶雕出的作品《寄畅园之冬》吸引了众多参观者的眼球.东海县是国家火炬计划硅材料产业化基地,产品有晶莹剔透的水晶制品,更有用途广泛的石英砂、石英玻璃、硅微粉等硅的系列产品.其中石英砂(主要成分为
)是制取高纯硅的主要原料,高纯硅又是制造计算机芯片的主要原料.资料卡:由石英砂制得高纯硅的反应原理为:
①
↑
②
③
其生产过程示意如下:
请你自学上述资料后,回答下列问题:
(1)由石英砂制得高纯硅的反应原理中,属于化合反应的是(填数字代号,下同),属于置换反应的是.
(2)粗硅提纯必须在无氧的氛围中进行,除了考虑到硅易被氧化成二氧化硅外,还有一个原因是.
(3)生产过程示意图中的"物质
"用水吸收,可得副产品(一种常见的酸)的名称是.
(4)作为电器、电子、光纤等行业原料的石英砂纯度要求高,需要对普通石英砂(含有少量的
)进行提纯,其中酸洗(用盐酸)和高纯水洗是两个重要的步骤.请写出酸洗步骤的一个反应的化学方程式:(任写一个);判断高纯水洗是否洗净的方法是取少量最后的洗涤液于试管中,向其中滴加
溶液,若无现象,则表明残留物已洗净;否则,表明残留物未洗净.
"低碳生活"是指生活作息时所耗用的能量要尽量减少,从而降低碳、特别是二氧化碳的排放量.上海世博会采用的1000余辆新能源汽车充分体现了"低碳"理念.汽车能源的更新历程如下:
(1)汽车用汽油、柴油作燃料,不完全燃烧时,会生成、碳氢化合物、氮的氧化物和烟尘等空气污染物,通常用催化转化的方法处理尾气,其反应原理用化学方程式表示为
,其中"
"的化学式为.
(2)最近,我市有千余辆公交和出租车完成了油改气(汽油改天然气),使港城人出行越来越"低碳",也为降低效应作出了有益的贡献.天然气的主要成分是,其在空气中完全燃烧的化学方程式为_.
(3)2004年4月,化学家研究发现,利用二氧化碳和环氧丙烷(
)在催化剂作用下可生成全降解塑料,环氧丙烷属于(填"有机物"或"无机物"),这不仅是体现"低碳"理念的又一举措,而且可以降低废弃塑料带来的问题.
2010年"世界水日"的主题是"关注水质、抓住机遇、应对挑战".了解水、爱护水、节约水是每个公民应尽的责任.
(1)水(填"属于"或"不属于")人类六大营养素之一;水属于化合物中的(填"氧化物"或"酸"或"碱"或"盐").水在日常生活中有着广泛的应用,下列应用正确的是(填数字代号).
①为了防止煤气中毒,可以在室内放一盆水②图书馆内图书着火,最好用水扑灭
③在生理盐水中,水是溶剂 ④长期饮用硬水是补钙的最好方法,有利于人体健康
⑤上海世博园将水雾化使之漂浮于空气中,以起降温作用
(2)据报道,我市人均水资源量仅为全国人均水资源量的14%,属于严重缺水的城市,并且地处淮河水系下游和入海口,污染水多.因此,节约用水和污水处理就显得尤为重要.
下列是保护市区主要供水河流--蔷薇河水质的建议,其中不正确的是(填数字代号).
①严禁将含磷废水排入河中②坚决杜绝岸边农田使用农药和化肥
③严禁在河边随意堆放生活垃圾④严禁在河边丢弃含汞、铅等金属的废旧电池
(3)生活中节约水的方法很多.如:用洗衣水冲厕所;请你再举一例:.