根据水泥和玻璃的生产,总结出硅酸盐工业的一般特点是 ( )。
①生成物是硅酸盐
②反应条件是高温
③含有硅的物质作原料
④反应原理是一系列复杂的物理—化学变化
| A.①③ | B.①②③ | C.①③④ | D.①②③④ |
11.在一个容积可变的密闭容器中发生反应:2X(s)+Y(g)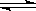 2Z(g)△H>0,欲加快正反应速率且提高Y的转化率,下列方法可行的是
2Z(g)△H>0,欲加快正反应速率且提高Y的转化率,下列方法可行的是
| A.保持容积不变,继续通入Y气体 |
| B.保持容积不变,及时移走Z气体 |
| C.压缩容器,而不改变物质状态 |
| D.保持容积不变,升高温度 |
10.在1L容器中充入0.5mol N2和1.5mol H2发生反应:N2(g)+3H2(g) 2NH3(g)ΔH ="-92.4" kJ•mol-1,下列关于该反应的说法正确的是
2NH3(g)ΔH ="-92.4" kJ•mol-1,下列关于该反应的说法正确的是
| A.反应达到平衡时共放出46.2 kJ的热量 |
| B.若将容器体积压缩至0.5L,可提高单位体积内活化分子百分数,从而加快正反应速率,降低逆反应速率 |
| C.任何时刻均有:υ(N2)=3υ(H2)=2υ(NH3) |
| D.若保持容器体积不变,继续通入0.5mol N2和1.5mol H2,则N2的转化率变大 |
9.下列事实不能用勒夏特列原理解释的是
| A.热的纯碱去污效果更好 |
| B.在H2、I2和HI组成的平衡体系加压后,混合气体颜色变深 |
| C.实验室可用排饱和食盐水的方法收集氯气 |
| D.高压下有利于提高合成氨的产率 |
8.在2NO2(红棕色)  N2O4(无色)的可逆反应中,下列状态一定达到化学平衡状态的是
N2O4(无色)的可逆反应中,下列状态一定达到化学平衡状态的是
| A.N2O4和NO2的分子数比为1︰2 |
| B.N2O4和NO2的浓度相等 |
| C.单位时间内1 mol N2O4消耗的同时有2 mol NO2生成 |
| D.平衡体系的颜色不再改变 |
7.下列事实中,与电化学腐蚀无关的是
| A.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀 |
| B.为保护海轮的船壳,常在船壳上镶入锌块 |
| C.在空气中,金属银的表面生成一层黑色物质 |
| D.镀银铁制品,镀层部分受损后,露出的铁表面易被腐蚀 |