为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:
请问:①操作Ⅰ的名称是 。要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和 ;
②若过滤所得固体未经洗涤即烘干称量,测得样品中氯化钠的质量分数将 。(填“偏大”“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为 g。(用a、b、c表示)
水是一种重要的资源。请回答下列问题:
(1)下列说法正确的是 (填序号)。
A.软水加入肥皂水容易起浮渣 B.生活中常用煮沸的方法降低水的硬度
C.活性炭在净水中起到吸附作用 D.自来水厂过沉淀、过滤、吸附、消毒等可将泉水变成纯净水
(2)如图所示为X、Y、Z三种固体物质的溶度曲线,请回答下列问题:
①t1℃时,三种物质溶解度的大小关系是 。
②要将t2℃时X的饱和溶液变成不饱和溶液,可采取的措施有:升高温度、 等。
③将t2℃时溶质质量分数为25%的X溶液降温到t1℃,所得溶液中溶质质量分数是 。

如图为A、B、C、D、E五种粒的结构示意图,请按要求填空:
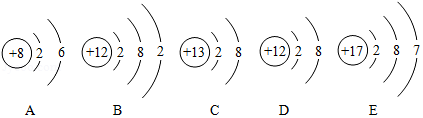
(1)A、B、C、D、E种粒子中,属于同种元素的是 (填序号)。
(2)E元素的原子在化学变化中容易形成 (填“阴离子”或“阳离子”)。
(3)由A元素和C元素形成的化合物的化学式为 。
请用合适的化学用语填空:
(1)3个氧原子
(2)铵根离子
(3)2个甲烷分子
(4)标出硝酸镁中镁元素的化合价
现有失去标签的四瓶溶液,分别是氯化铁、氯化钙、稀盐酸、氯化钠溶液中的一种,为了鉴别出它们,进行以下实验,实验步骤及现象如下:
(1)通过观察,溶液呈黄色的是 .
(2)将剩余溶液分别取样,加入 溶液,可以将它们一次性鉴别出来.
已知A、B、C、D是初中化学常见的四种物质,在一定条件下它们之间的关系如图(部分物质及反应条件己略去).其中B、C是组成元素相同的气体,D是目前世界年产量最高的金属,A是黑色固体,请回答:
(1)写出下列物质的化学式:A ;B .
(2)C在工业上常用来冶炼D,写出其反应的化学方程式 ,在这个反应中, ___发生了氧化反应.
